|
The Korean text of this paper can be translated into multiple languages on the website of http://jksee.or.kr through Google Translator.
AbstractIn this study, the occurrence and temporal variation of eight pharmaceuticals comprising antibiotics (clarithromycin, sulfathiazole, sulfamethazine, sulfamethoxazole, trimethoprim), scabicide (carbamazepine) and nonsteroidal anti-inflammatory drugs (acetylsalicylic acid, naproxen) in main stream and its tributary of the Nakdong River basin, were investigated. Concentrations of the target compounds ranged from <LOQ to 1.076 μg/L. The highest average concentration was observed for clarithromycin (0.0316 μg/L), followed by sulfamethazine (0.0170 μg/L), sulfamethoxazole (0.0161 μg/L), naproxen (0.0129 μg/L), carbamazepine (0.0093 μg/L), acetylsalicylic acid (0.0047 μg/L), sulfathiazole (0.0024 μg/L) and trimethoprim (0.0022 μg/L). The decreasing pattern of pharmaceutical concentrations was observed along with Nakdong River and the higher concentrations in downstream were observed than those in upstream. There was no temporal variation of the target compounds although the highest level was found in February. The calculated hazard quotients (HQs) for eight pharmaceuticals were below 1, indicating no environmental hazard in Nakdong River. However, further monitoring is still needed due to the other pharmaceuticals widely used in Korea.
요약본 연구는 낙동강 본류와 연계한 지천중심을 대상으로 항생제(clarithromycin, sulfathiazole, sulfamethazine, sulfamethoxazole, trimethoprim), 항정간제(carbamazepine), 진통제(acetylsalicylic acid, naproxe)를 포함한 8종의 의약물질의 현황 및 시기별 변화에 대해 조사를 실시하였다. 조사 대상물질의 검출 수준은 <LOQ에서 1.076 μg/L까지 나타났으며, 조사 대상물질에서 clarithromycin (0.0316 μg/L)이 가장 높은 평균 농도로 검출되었고, 다음으로 sulfamethazine (0.0170 μg/L), sulfamethoxazole (0.0161 μg/L), naproxen (0.0129 μg/L), carbamazepine (0.0093 μg/L), acetylsalicylic acid (0.0047 μg/L), sulfathiazole (0.0024 μg/L), trimethoprim (0.0022 μg/L) 순으로 나타났다. 낙동강 수계의 지점별 검출 수준은 하류의 농도수준이 상류의 검출 농도보다 상대적으로 높게 나타났다. 2월 조사시기에서 높은 검출 수준을 보였으나, 시기별 차이는 뚜렷하게 나타나지 않았다. 대상 의약물질 8종의 유해지수를 산정한 결과 모두 1보다 낮은 값을 나타내어 낙동강 수계에 미치는 생태위해성은 낮은 것으로 평가되었으나 추후 본 연구대상 물질 외 사용되고 있는 다른 의약물질로 확장 한 연구가 더 수행될 필요가 있는 것으로 판단된다.
1. 서 론의약물질은 질병의 예방, 진단, 치료 등을 목적으로 개발된 물질로 산업화와 함께 인간의 활동이 다양해지면서 인체, 동물, 수산물 양식과 농산물 생산 등에 광범위하게 사용되고 있다. 이러한 의약물질의 사용량은 고령화 사회가 심화함에 따라 증가하고 있다[1]. 국내 통계청에 따르면 2010년 노령화 지수가 68.0에서 2015년에는 95.1로 증가하고 있으며, 2015년 기준으로 65세 이상 노령인구가 654만 명으로 전체 인구의 11%를 차지하고 2026년에는 20.8%까지 증가할 전망이다[2]. 또한, 인구가 도시에 집중되어 수도권에 전체 인구의 약 50%인 2,511만 명, 부산 986만 명, 대구 245만 명이 거주하면서[3] 의약물질의 사용량이 도심지역에 집중되어 도심 인근 환경(하․폐수처리장, 하천수, 지하수, 토양 등)에서 지속해서 검출될 것으로 예상한다. 한국제약협회의 조사에 따르면 2009년 국내에 유통되는 인체용 의약물질의 주요 성분은 약 1,000여 종으로 약 16,000여 가지 이상의 제품으로 생산 및 유통되고 있다[4]. 2015년 전체 의약물질 생산 금액 가운데 순환계용 약이 18%로 가장 높은 비율을 차지하였고 다음으로 중추신경계용 약이 13%를 차지하였다. 항생물질제제 및 화학요법제 의약물질은 각각 8%, 3%로 나타났다[5]. 국내 선행연구에서 2007년 의약물질의 생산량을 추정산정한 결과 naproxen (69,274 kg), acetylsalicylic acid (57,409 kg), clarithromycin (54,843 kg), sulfamethoxazole (12,296 kg), carbamazepine (8,897 kg)로 보고된 바 있으며, 국내 수계에서 해당 물질의 검출이 지속해서 보고되고 있다[6-12].
의약물질은 생산공정 및 저장과정에서 유출되거나 도시 하수, 축산 폐수 등과 같이 다양한 유입 경로를 통해 상수원인 강이나 호소로 유입되어 잔류하며, 장시간 생물학적 활성을 가지면서 수중에 존재하여 생태계 내에 잠재적 위해성을 가지는 것으로 알려져 있다[13~15]. 유럽 의약청(European Medicines Agency, EMEA) 및 미국 식품의약국(Food and Drug Administration, FDA)은 의약물질에 대한 환경 위해성 평가를 위해 수 생태계에서 독성 농도 기준을 1 μg/L로 제시하고 있다[16~18]. 국내의 경우 의약물질의 수계 내 규제 기준은 미비한 실정이며 의약물질 규제 기준을 설정하기 위한 기반 연구인 모니터링 연구들이 수행되고 있다.
본 연구의 조사대상 지역인 낙동강은 부산, 울산, 경상남도지역 주민들의 상수원으로 전체 52개소 취수장에서 평균 931,369 m3/일의 정수를 생산 및 공급하는 주요 상수원이다[19]. 낙동강은 대구, 구미의 공업단지에서 배출된 유해 화학물질로 인한 수질오염 사고가 발생할 가능성이 높으며[20~23], 2015년 전국 오염원 조사에서 낙동강 수계로 배출되는 환경기초시설은 약 420개소로 하수처리시설(2,426,000 m3/일), 마을 및 공공 하수도(11,000 m3/일), 폐수처리시설(151,000 m3/일) 등 다양한 오염원으로부터 배출된 미량 유해오염물질이 낙동강 수계에 잠재적 영향을 줄 수 있다[24]. 이에 낙동강 수계의 안전한 상수원을 보호를 위한 모니터링 연구가 필요로 한다.
따라서 본 연구에서는 공단, 도시하천 등의 낙동강 중권역 대표지점으로 유입되는 지천 20개 지점을 대상으로 의약물질의 검출 수준과 시기별(2월, 4월, 6월, 8월) 분포 패턴을 파악하고자 하였으며, 안전 계수를 이용하여 예측무영향농도(Predicted no effect concentration, PNEC)를 계산하여 검출된 의약물질이 낙동강 수계에 미치는 위해성을 파악해 보고자 하였다.
2. 연구방법2.1. 조사대상 물질본 연구에서는 의약물질 중 진통제 2종(acetylsalicylic acid, naproxen), 항생제 5종(clarithromycin, sulfamethazine, sulfamethoxazole, sulfathiazole, trimethoprim), 항정간제 1종(carbamazepine)을 포함한 8종의 의약물질을 대상 물질로 선정하여 분석하였다.
2.2. 시약 및 기기본 연구에서 사용된 표준물질(acetylsalicylic acid, carbamazepine, clarithromycin, naproxen, sulfamethazine, sulfamethoxazole, sulfathiazole, trimethoprim) 및 내부표준물질(sulfamethazine-13C6, sulfamethoxazole-13C6, sulfathiazole-13C6, trimethoprim-d9, ibuprofen-d3, clarithromycin-M-methyl-d3)은 Sigma-Aldrich (St Louis, MO, USA)사에서 단일 물질로 만들어진 시약을 구매하여 희석하여 사용하였으며, Milli-Q water, 메탄올(methanol), 아세토니트릴(acetonitrile)은 J.T Baker (Phillipsburg, NJ, USA)사의 HPLC 등급 이상의 용매를 사용하였다. 포름산(formic acid), 포름산 암모늄(ammonium formate), 아세트산(acetic acid), 암모늄 아세테이트(ammonium acetate), 황산(H2SO4), 에틸렌다이아민테트라아세트산(Ethylenediaminetetraacetic acid; EDTA)등의 시약은 Wako (Osaka, Japen), PFP (MATSUNOEN Chemical LTD, Japen), Yakuri (Kyoto, Japen)사의 특급시약을 이용하였다. 시료의 정제 및 추출을 위한 카트리지로는 OASIS HLB (200 mg, 6 cc; Waters)를 이용하였다. 시료의 정제 및 추출을 위한 고체상 추출(solid phase extraction, SPE)장치로는 Supelco (Bellefonte In, PA, USA)의 VisiprepTM SPE Vacuum manifold를 사용하였다. 기기분석에는 액체크로마토그래프-텐덤질량분석기(LC-MS/MS)를 이용하였으며, Agilent사의 1200 series 액체크로마토그래프(LC)와 Agilent사의 6460 triple quadrupole mass spectrometer를 검출기로 사용하였다. 가드 컬럼은 Agilent사의 4.6 mm × 12.5 mm, 5 μm pore size와 컬럼은 4.6 mm × 150 mm, 3.5 μm pore size의 ZORBAX Eclipes XDB-C18을 사용하였다.
2.3. 시료채취 및 조사주기시료 채취는 낙동강유역환경청 수질 측정망 운영계획을 참고하여 낙동강 본류와 연계한 지천중심(제1지류) 대상으로 20개 지점을 실시하였으며, 각 채취지점은 아래 Fig. 1에 나타내었다. 시료 채취는 EPA Protocol에 따라 하천 조사지점은 중앙부위에서 채수하였고, 유해 유기물질 시료 용기는 국제적으로 공인된 1 L 갈색 유리병(ESS사 제품)에 채수하였으며, 헤드 스페이스 없이 채취하여 모든 채수된 시료 용기는 아이스팩과 함께 아이스박스에 담아 당일 실험실로 이송하여 분석 직전까지 4℃에서 냉장 보관하였다. 모든 분석은 채취 일주일 이내에 실시하였다. 시료 채취는 2016년 2월부터 8월에 거쳐 연 4회 실시하였으며, 1차 조사는 2월, 2차 조사는 4월, 3차 조사는 6월, 4차 조사는 8월에 실시하였다.
2.4. 실험방법의약물질 8종(acetylsalicylic acid, carbamazepine, clarithromycin, naproxen, sulfamethazine, sulfamethoxazole, sulfathiazole, trimethoprim)의 분석은 GFF (Glass microfiber filters)로 여과한 시료 500 mL를 취하여 6 N 황산을 사용해 시료의 pH를 2로 조절한 후 EDTA 40 μg을 넣고 내부표준물질(acetylsalicylic acid-d3, sulfamethazine-13C6, sulfamethoxazole-13C6, sulfathiazole-13C6, trimethoprim-d9) 50 ng을 첨가하였다. SPE 장치에 HLB (200 mg, 6 cc) 카트리지를 장착한 후 메탄올, pH 2로 조절된 Milli-Q water 각 12 mL를 차례로 통과시켜 컨디셔닝하였다. 이후 카트리지에 시료를 8~10 mL/min의 속도로 적재하고, 시료의 적재가 끝난 카트리지는 약 30분간 진공 감압펌프를 이용하여 건조한 다음 메탄올 12 mL로 용리시켰다. 이 용리액을 질소농축기(Turbu vap LP, Caliper life sciences, Hopkinton, USA)를 사용하여 농축시키고, 아세토니트릴과 메탄올을 이용하여 재 용해시켜 0.45 μm PTFE (Polytetrafluoroethylene) 시린지 필터로 여과시킨 후 최종 부피를 1 mL가 되도록 하였다. LC-MS/MS로 기기분석을 위해 이동상으로 positive mode에서 acetonitrile/methanol (50:50, v/v%)와 0.3% ammonium formate, 0.1% formic acid를 사용하였고, negative mode에서 acetonitrile/methanol (50:50, v/v%)와 0.3% ammonium acetate, 0.1% acetic acid를 사용하였다. 각 의약물질의 전구이온(precursor ion)과 생성이온(product ion)을 선정하여 다중 반응 모니터링(multiple reaction monitoring, MRM) 기능으로 분석하였다(Table 1).
2.5. 정도관리분석법에 대한 정량 한계(Limit of quantitation, LOQ)는 하천수 500 mL에 10 ng 혼합표준물질을 첨가 후 동일한 전처리 과정을 7회 반복 실험하여 얻은 분석값 결과의 표준편차에 10을 곱한 값으로 산정하였다. 결과 정량한계는 acetylsalicylic acid 0.0169 μg/L, carbamazepine 0.0061 μg/L, clarithromycin 0.0096 μg/L, naproxen 0.0096 μg/L, sulfamethazine 0.0022 μg/L, sulfamethoxazole 0.0031 μg/L, sulfathiazole 0.0025 μg/L, trimethoprim 0.0038 μg/L로 각각 나타났다. 하천수 500 mL에 혼합표준물질을 20 ng 첨가하여 5회 반복 실험하여 얻은 정확도는 acetylsalicylic acid 105%, carbamazepine 123%, clarithromycin 104%, naproxen 103%, sulfamethazine 96%, sulfamethoxazole 100%, sulfathiazole 100%, trimethoprim 98%였으며, 정밀도는 acetylsalicylic acid 12.6%, carbamazepine 1.6%, clarithromycin 3.4%, naproxen 0.7%, sulfamethazine 4.6%, sulfamethoxazole 1.7%, sulfathiazole 3.0%, trimethoprim 5.3%로 각각 나타났다.
2.6. 위해성 평가국내외 문헌 조사를 통해 위해성 평가를 위한 8종 의약물질에 대한 생태 독성자료를 아래 Table 2에 나타내었다. 조사된 생태독성자료 중 가장 민감한 생물종에 해당하는 독성 값을 선택하였으며, 안전계수는 EC 위해성 평가 핸드북의 정보를 참고하여[25] 예측무영향농도(PNEC)를 식 (1)을 통해 산출하였다.
여기서, AF: 안전계수(assessment factor)
이에 근거하여 본 연구의 실측환경농도의 평균과 95% 상한 신뢰구간을 대푯값으로 사용하여 예측무영향농도를 토대로 유해지수(HQs)를 식 (2)를 통해 산출하였다.
여기서,
MEC: 실측환경농도(measured environmental concentration)
PNEC: 예측무영향환경농도(predicted no effect concentration)
유해지수 값이 1 이상일 경우, 환경 중에 유해물질이 생태계에 부정적인 영향을 미칠 가능성이 존재한다는 것으로 의미하며 유해지수 값이 1 보다 낮은 경우에는 생태위해성이 낮은 것으로 판단할 수 있다[13].
3. 결과 및 고찰3.1. 전체 농도 수준낙동강 본류와 연계한 지천 중심 대상으로 20개 지점에서 분석한 8종 의약물질의 조사시기별 농도수준 및 검출빈도는 다음 Fig. 2에 나타내었다. 전체 대상 의약물질 중 clarithromycin이 20-65%의 검출빈도와 평균 0.0316 μg/L로 높은 검출 수준을 보였으며, trimethoprim은 5-30%의 검출빈도 및 평균 0.0022 μg/L로 다른 물질에 비해 상대적으로 낮은 수준으로 검출되었다. 대부분 물질이 8월보다 2월 조사에서 높게 검출되는 경향을 보였으나, acetylsalicylic acid은 반대로 8월 조사에서 2배 정도 높게 나타났다.
국내외 수계에서의 의약물질 농도 수준은 다음 Table 3과 같다. 국외의 경우, 대부분의 의약물질의 농도 수준이 유사한 경향성을 보이며, 포르투갈의 경우 조사 지점이 하수처리장 인근 호수에서 시행되어 본 연구결과보다 상대적으로 다소 높게 나타났다[38]. 국내의 경우, 2008-2011년 국립환경과학원에서 수행한 4대강 의약물질 조사에서 상대적으로 금강이 다소 높게 검출된 바 있으나, 대부분의 수계 내 농도 수준은 유사한 경향성을 나타났다[10,12,39,40]. 2011년 낙동강 수계에서[12] acetylsalicylic acid가 최대 1.181 μg/L로 검출된 바 있고, 본 연구에서 sulfamethazine이 밀양강 지점에서 1.076 μg/L로 높게 검출된 것을 제외하면 낙동강 수계 내 의약물질의 연도별 농도 경향성은 유사하거나 다소 감소하는 것을 볼 수 있다.
3.2. 농도수준 및 검출분포3.2.1. 조사 지점별 분포낙동강 수계 지천 중심으로 20개 지점을 총 4회에 걸쳐 조사한 의약물질의 지점별 농도 수준과 분포패턴을 임하댐 인근에서 안동댐 하류구간(1-2)을 낙동강 상류로, 내성천 인근부터 회천구간(3-11)을 낙동강 중류로, 차천 인근에서 서낙동강구간(12-20)을 하류로 분류하여 농도 및 분포 패턴을 Fig. 3에 나타내었다.
상류에서 평균 ND-0.0016 μg/L로 검출되며, 지점1(반변천)에서 모든 물질이 검출되지 않았으며, 지점2(미천)에서 carbamazepine (0.0083 μg/L), sulfamethoxazole (0.0041 μg/L)이 검출되었다. 지점3(내성천) 인근부터 중류에서는 평균 0.0020-0.0891 μg/L, 하류에서는 평균 0.0029-0.1768 μg/L로 상류보다 다소 높은 수준을 나타났다. 특히 지점20(서낙동강)에서 0.1183 (ND-0.5651) μg/L 수준으로 낙동강 지류 가운데 가장 높은 농도를 나타내었다. 낙동강 하구에 위치한 해당 지점은 2012년 기준 하수처리장 6개소(376,500 m3/일), 분뇨 처리시설 3개소(3,880 m3/일), 마을 하수도 7개소(890 m3/일), 산업 폐수처리시설 3개소(30,270 m3/일), 매립장 침출수 3개소(27,451 m3/일)가 인근에 있으며[44,45], 서낙동강 지점은 낙동강 중권역의 오염도가 높은 지점 중 하나로 중점관리대상 지역으로 선정되어 조사된바 있으며[46], 이전 선행 연구에서도 해당 지점에서 농약류의 검출 수준이 높게 나타난 바 있다[47]. 다음으로 지점11(금호강)에서 0.0891(ND-0.348) μg/L 수준으로 높게 검출되었으며, 해당 지점은 금호강과 낙동강 지류가 만나는 지점으로 금호강 내 오염물질들이 낙동강으로 유입되어 낙동강 수계가 오염될 우려가 크다. 금호강의 환경기초시설은 하수처리장 10개소(1,409,450 m3/일), 폐수처리장 2개소(100,200 m3/일), 축산 폐수처리장 1개소(180 m3/일)가 있다[48]. 금호강의 환경기초 시설들에서 배출된 방류수는 낙동강의 주 오염원으로 간주되고 있으며, 금호강 하류에서 낙동강 본류로 유입되는 지점에서 과불화합물과 농약류에 의한 오염도가 높게 확인된 바 있다[47,49]. 각 조사지점에서 검출되는 경향성은 뚜렷하게 나타나지 않으나, 상류(평균: 0.0008 μg/L)보다 중류(0.0416 μg/L)와 하류(0.0650 μg/L)에서 최대 60배 높은 수준으로 나타나며 Mann-Whitney 검증 결과, 상류와 중류, 상류와 하류 간에 유의미한 차이(p<0.05)를 나타났다.
3.2.2. 조사 시기별 분포2월부터 8월까지 4회(2월, 4월, 6월, 8월)에 걸쳐 조사한 결과의 농도 및 분포 패턴을 Fig. 4에 나타내었다. 총 의약물질 농도의 시기별 경향성은 2월(중간값: 0.0694 μg/L) > 4월(중간값: 0.0361 μg/L) > 6월(중간값: 0.0148 μg/L) > 8월(중간값: 0.0147 μg/L)의 순서로 나타났으며 Mann-Whitney 검정 결과, 2월과 6월, 2월과 8월 조사 간에 유의미한 차이(p < 0.05)를 나타났다. 상류, 중류, 하류로 다시 구분하여 조사 시기별 차이를 확인한 결과 중류에서만 2월과 8월 조사에서 유의미한 차이(p = 0.012)를 나타났다. 계절별 항생제 검출은 2월이 8월보다 높은 검출빈도 및 농도로 검출되었으며, Mann-Whitney 검정 결과 중류에서만 2월과 8월 조사 간에 유의미한 차이(p < 0.05)를 나타났다. 조사 시기 당시의 평균 강수량은 각각 43.8 mm, (2월), 158.1 mm (4월), 67.4 mm (6월), 76.2 mm (8월)이었으며[50], Pearson 상관분석 결과 강수량과 시기별 농도는 서로 상관관계가 없는 것으로 나타났다. 이전 선행연구에 의하면 계절에 따라 유량이 많은 시기에 의약물질이 낮은 농도로 검출된 바 있다[51]. 2월 조사에서 clarithromycin이 전체 농도에서 53%를 차지하면서 우세하게 검출되었으나 8월 조사에서는 13%로 감소하였다. Clarithromycin은 약효군별 분류에서 기타의 항생물질제제(약효분류코드 619)로 분류되고, 콧물, 기침 등을 동반하는 급성 인후염을 치료하는 항생제로 amoxicillin/clavulanate (46.2%) 다음으로 clarithromycin (10.4%)이 많이 처방되고 있다[52]. 건강보험심사평원의 통계에 따르면 항생제 및 해열․진통․소염제의 2016년 2월 처방일수는 466,820일로 8월의 처방일수 382,274일보다 높아 겨울에 이들 약품의 사용량이 많다[53]. 또한, 의약물질의 하수처리장에서 제거효율은 수온, 일사량 등 환경적 요인에 영향을 받아 겨울보다 여름의 제거효율이 높으며, 겨울에 상대적으로 높게 검출된 바 있다[54,55].
3.3. 의약물질 낙동강 수계 위해성 평가미국 FDA와 유럽 EMEA의 가이드라인에서 신규 의약물질에 대한 승인 시 해당 의약물질의 사용에 따른 하수처리시설의 최소 수생태계 독성 농도를 1 μg/L로 정하고 이를 초과할 경우 수생태계 독성평가 자료에 근거하여 PNEC 등 환경성 평가 자료를 추가 요청하고 있다. 이에 본 연구에서 조사한 8종의 의약물질이 수생태계에 미치는 독성영향을 평가하기 위하여 수질독성을 평가한 자료에서 얻은 예상무영향농도와 실측된 환경 중 농도를 비교하여 유해지수를 산출한 결과는 위의 Table 4와 같다. 선행연구에서 수행된 생태독성자료 중 높은 독성값에 근거하여 PNEC값을 산출한 결과 clarithromycin이 0.23 μg/L로 조사대상 물질 중 가장 낮은 무영향농도값을 나타내었다. 실측된 농도값의 95% 상한 신뢰구간 값에 근거하여 산출된 유해지수에서 clarithromycin (2.1.E-01)이 가장 높게 산출되었고 다음으로 sulfamethoxazole (2.1.E-02), sulfamethazine (5.2.E-03), carbamazepine (8.9.E-04), naproxen (5.3.E-04), acetylsalicylic acid (1.2.E-04), trimethoprim (7.0.E-05), sulfathiazole (5.0.E-05)로 모든 물질의 유해지수가 1보다 낮은 것으로 나타났다. 일부 지점에서 1.076 μg/L수준으로 검출된 것을 제외하고, 미국 FDA이 선정한 의약물질의 수생태계 독성 농도인 1 μg/L보다 낮은 수준으로 검출되었다. 본 연구는 국외 선행연구보다 상대적으로 낮은 HQs값을 나타났다[56,57]. 일반적으로 하수처리장 방류수보다 지표수에서 HQs값이 낮게 나타나며, 이는 방류수가 하천으로 유입되어 희석된 것으로 확인된다[58]. 본 연구에서 낙동강 수계 내 잔류 의약물질의 오염 수준은 수생태계에 위해를 초래할 수준은 아닌 것으로 판단되나 혼합독성으로 인한 위해성을 고려하지 않아 추후 이에 관한 연구도 수행될 필요가 있는 것으로 판단된다.
4. 결 론본 연구는 낙동강 본류와 연계한 지천중심으로 20개 지점을 대상으로 진통제, 항생제, 항전간제를 포함한 8종의 의약물질을 4회(2월, 4월, 6월, 8월)에 걸쳐 조사하여 다음과 같은 결과를 얻었다. 시기별 조사에서 전체적으로 의약물질의 사용량이 높은 겨울(2월)이 상대적으로 높은 농도 수준을 나타났으며, 8종의 의약물질 가운데 clarithromycin이 높게 검출되었다. 대도시와 공업단지, 환경기초시설 현황 등 오염배출원이 많이 위치한 중․하류에서 높게 검출되는 것을 확인하였다. 수계 내 실측된 의약물질의 농도로 수행한 단일 물질별 위해성 평가 결과 HQs < 1로 낮은 것으로 나타났으나 본 조사대상인 8개 의약물질 외 많은 의약물질이 사용되고 있으므로 추후 조사 대상물질을 확대한 모니터링 및 위해성 평가 연구가 수행될 필요가 있다.
Acknowledgments이 연구는 낙동강수계관리위원회의 2016년 낙동강수계 환경기초사업의 지원 및 2017년도 정부(미래창조과학부)의 재원으로 한국연구재단의 지원을 받아 수행된 연구임(NRF-2015R1C1A2A01051544).
Fig. 2.Mean concentration and detection frequency of each target pharmaceutical with sampling period. 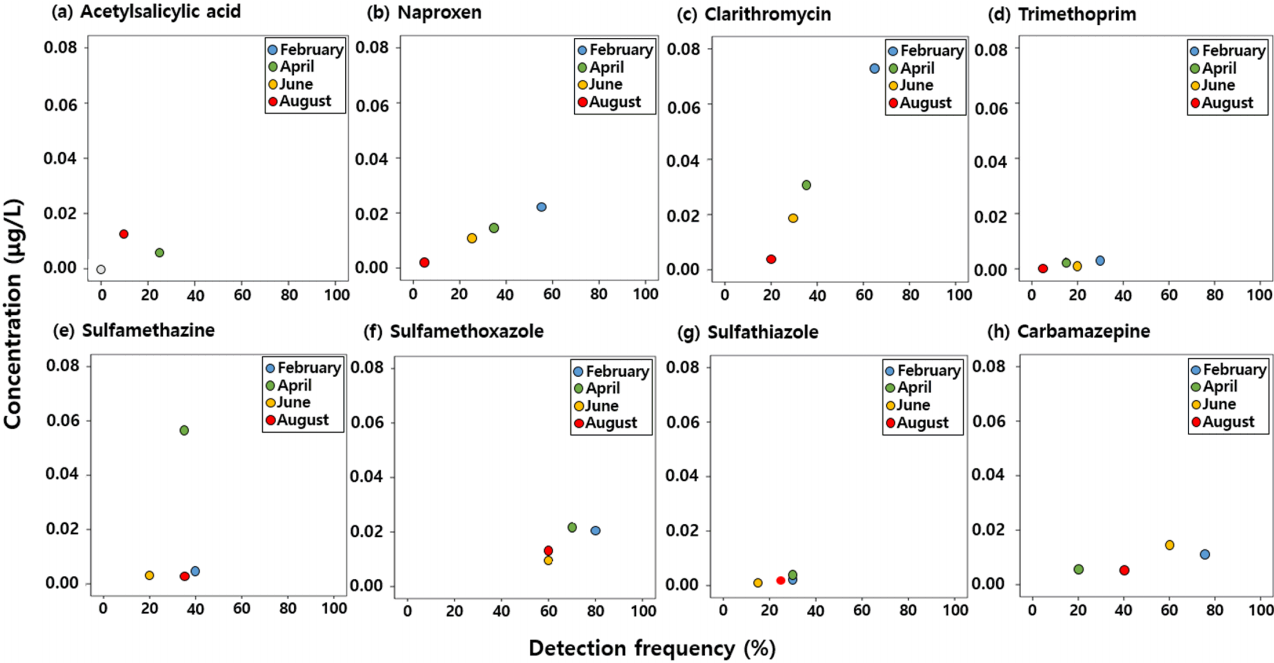
Fig. 3.(a) Box plot for the total concentration of pharmaceuticals with sampling sites (red bar; mean concentration, black bar; median concentration) (b) Distribution patterns of pharmaceuticals in each sampling site. 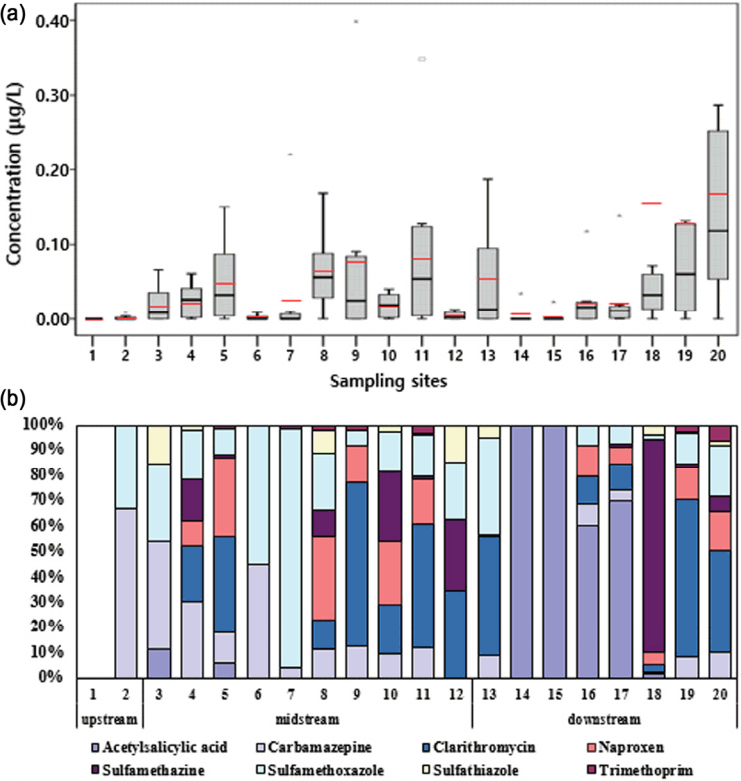
Fig. 4.(a) Box plot for total pharmaceutical concentrations in each sampling period (red bar; mean concentration, black bar; median concentration) (b) Distribution patterns of pharmaceuticals in seasonal samples. 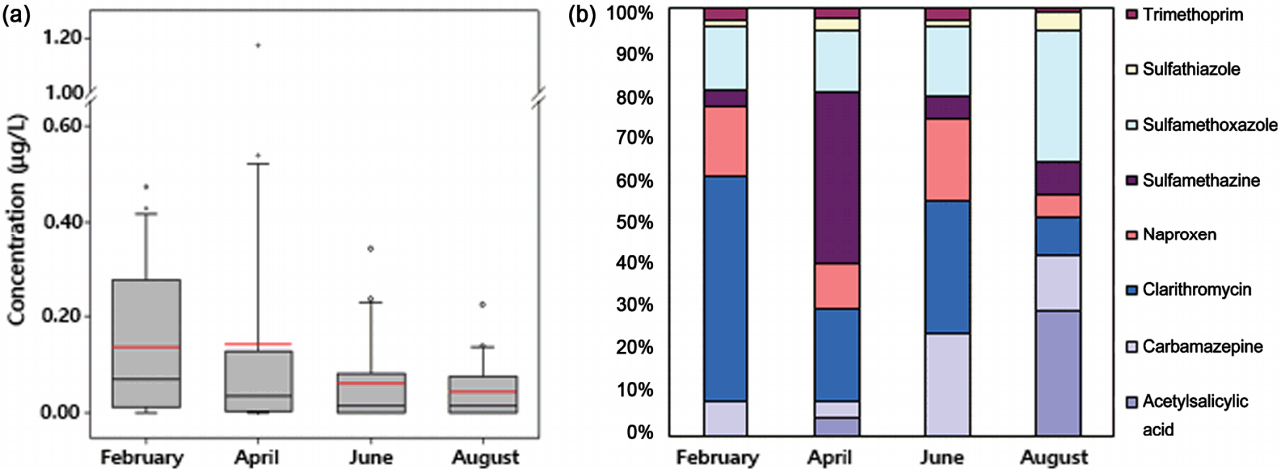
Table 1.Multiple reaction monitoring (MRM) conditions Table 2.L(E)C50 (in mg/L) of target pharmceuticals
Table 3.Comparison of pharmaceuticals concentrations (μg/L) in river water of this study with other previous studies
Table 4.The hazard quotients (HQs) obtained from the measured environmental concentration (MEC) in this study
References1. Korea Institue for Health and Social Affairs (KIHASA), “The Development of Health Care System for Older Koreans,” Research Report 2005-04(2005).
3. Statistics Korea Home Page, http://www.index.go.kr/potal/main/EachDtlPageDetail.do?idx_cd=1007, March(2017)
4. Korea Pharmaceutical Manufacturers Association (KPMA), Pharmaceutical production in 2009, (2010).
5. Ministry of Food and Drug Safety (MFDS) Home Page, http://www.mfds.go.kr/index.do?mid=1577&area=04, March(2017)
6. National Institute of Environmental Research (NIER), Development of Analytical Method and Study of Residual Pharmaceuticals(I), (2008).
7. National Institute of Environmental Research (NIER), Development of Analytical Method and Study of Residual Pharmaceuticals(II), (2009).
8. National Institute of Environmental Research (NIER), Development of Analytical Method and Study of Residual Pharmaceuticals(III), (2010).
9. National Institute of Environmental Research (NIER), Development of Analytical Method and Study of Residual Pharmaceuticals(IV), (2011).
10. B. F.. Da Silva, A.. Jelic, R.. López-Serna, A. A.. Mozeto, M.. Petrovic, D.. Barceló, Occurrence and distribution of pharmaceuticals in surface water, suspended solids and sediments of the Ebro river basin, Spain, Chemosphere., 85(8), 1331-1339(2011).
11. Y.. Yoon, J.. Ryu, J.. Oh, B. G.. Choi, S. A.. Snyder, Occurrence of endocrine disrupting compounds, pharmaceuticals, and personal care products in the Han River (Seoul, South Korea), Sci. Total Environ., 408(3), 636-643(2010).
12. W. J.. Sim, J. W.. Lee, J. E.. Oh, Occurrence and fate of pharmaceuticals in wastewater treatment plants and rivers in Korea, Environ. Pollut., 158(5), 1938-1947(2010).
13. D. W.. Kolpin, E. T.. Furlong, M. T.. Meyer, E. M.. Thurman, S. D.. Zaugg, L. B.. Barber, H. T.. Buxton, Pharmaceuticals, hormones, and other organic wastewater contaminants in US streams, 1999-2000: A national reconnaissance, Environ. Sci. & Technol., 36(6), 1202-1211(2002).
14. C.. Carlsson, A. K.. Johansson, G.. Alvan, K.. Bergman, T.. Kühler, Are pharmaceuticals potent environmental pollutants?: Part I: Environmental risk assessments of selected active pharmaceutical ingredients, Sci. Total Environ., 364(1), 67-87(2006).
15. K.. Fent, A. A.. Weston, D.. Caminada, Ecotoxicology of human pharmaceuticals, Aquat. Toxicol., 76(2), 122-159(2006).
16. J. P.. Bound, N.. Voulvoulis, Pharmaceuticals in the aquatic environment -- a comparison of risk assessment strategies, Chemosphere., 56(11), 1143-1155(2004).
17. EMEA, Note for Guidance on Environmental Risk Assessment of Medicinal Products for Human UseCPMP/SWP/4447/00 draft corr2006.
18. FDA, Guidance for industry Environmental assessment of human drugs and biologics applicationsFDA, CDER/CBER, CMC 6, rev.11998.
19. Nakdong River Basin Environmental Office Home Page, https://www.me.go.kr/ndg/web/main.do, March(2017)
20. G. A.. Kim, C. D.. Seo, S. W.. Lee, D. C.. Ryu, K. W.. Kwon, Monitoring of Hazardous Chemicals for Effluents of STPs and WWTP in the Nakdong River Basin, J. Environ. Sci. Int., 23(7), 1253-1268(2014).
21. C. G.. Park, The problems and countermeasures of the water management in Nakdong river (in Korean), Nakdong River Res., 4, 4-13(2007).
22. I. J.. Lee, C. G.. Lee, S. N... Heo, J. G.. Lee, H. R.. Kim, D. S.. Yang, Y. H.. Lee, Monitoring of hazardous chemicals for wastewater discharge facilities in the Nakdong River basin, J. Korean Soc. Environ. Anal., 14(3), 128-136(2011).
23. J. J.. Yu, Management Strategy of Trace Hazardous Compounds in Nakdong River, J. Korean Soc. Environ. Eng., 31(6), 412-416(2009).
24. National Institute of Environmental Research (NIER) Home Page, https://wems.nier.go.kr/, April(2017)
25. TGD, E. U. Technical guidance document on risk assessment in support of commission directive 93/67/EEC on risk assessment for new notified substances, Commission Regulation (EC) No 1488/94 on Risk Assessment for existing substances, and Directive 98/8/EC of the European Parliament and of the Council concerning the placing of biocidal products on the market. Part I-IVEuropean Chemicals Bureau (ECB), JRC-Ispra (VA), Italy, April 2003. Part II. European Commission Joint Research Centre. EUR, 20418(2003).
26. M.. Cleuvers, Mixture toxicity of the anti-inflammatory drugs diclofenac, ibuprofen, naproxen, and acetylsalicylic acid, Ecotoxicol. and Environ. Saf., 59(3), 309-315(2004).
27. E.. Prášková, D.. Živná, S.. Štěpánová, M.. Ševčíková, J.. Blahová, P.. Maršálek, Z.. Svobodová, Acute toxicity of acetylsalicylic acid to juvenile and embryonic stages of Danio rerio, Neuroendocrinol. Lett., 33, 72-76(2012).
28. A.. Jos, G.. Repetto, J. C.. Rios, M. J.. Hazen, M. L.. Molero, A.. Del Peso, A.. Cameán, Ecotoxicological evaluation of carbamazepine using six different model systems with eighteen endpoints, Toxicol. in Vitro., 17(5), 525-532(2003).
29. V. L.. Cunningham, M.. Buzby, T.. Hutchinson, F.. Mastrocco, N.. Parke, N.. Roden, Effects of human pharmaceuticals on aquatic life: Next steps, Environ. Sci. Technol., 40, 3456-3462(2006).
30. Z. H.. Li, V.. Zlabek, J.. Velisek, R.. Grabic, J.. Machova, J.. Kolarova, T.. Randak, Acute toxicity of carbamazepine to juvenile rainbow trout (Oncorhynchus mykiss): effects on antioxidant responses, hematological parameters and hepatic EROD, Ecotoxicol. and Environ. saf., 74(3), 319-327(2011).
31. L.. Minguez, J.. Pedelucq, E.. Farcy, C.. Ballandonne, H.. Budzinski, M. P.. Halm-Lemeille, Toxicities of 48 pharmaceuticals and their freshwater and marine environmental assessment in northwestern France, Environ. Sci. and Pollut. Res., 23(6), 4992-5001(2016).
32. M.. Isidori, M.. Lavorgna, A.. Nardelli, L.. Pascarella, A.. Parrella, Toxic and genotoxic evaluation of six antibiotics on non-target organisms, Sci. Total Environ., 346(1), 87-98(2005).
33. J. O.. Straub, K. M.. Stewart, Deterministic and probabilistic acute-based environmental risk assessment for naproxen for Western Europe, Environ. Toxicol. and Chem., 26(4), 795-806(2007).
34. L. H.. Yang, G. G.. Ying, H. C.. Su, J. L.. Stauber, M. S.. Adams, M. T.. Binet, Growth-inhibiting effects of 12 antibacterial agents and their mixtures on the freshwater microalga pseudokirchneriella subcapitata, Environ. Toxicol. and Chem., 27(5), 1201-1208(2008).
35. J.. Jung, Y.. Kim, J.. Kim, D. H.. Jeong, K.. Choi, Environmental levels of ultraviolet light potentiate the toxicity of sulfonamide antibiotics in Daphnia magna, Ecotoxicol., 17(1), 37-45(2008).
36. Y.. Kim, K.. Choi, J.. Jung, S.. Park, P. G.. Kim, J.. Park, Aquatic toxicity of acetaminophen, carbamazepine, cimetidine, diltiazem and six major sulfonamides, and their potential ecological risks in Korea, Environ. Int., 33(3), 370-375(2007).
37. S.. Park, K.. Choi, Hazard assessment of commonly used agricultural antibiotics on aquatic ecosystems, Ecotoxicol., 17(6), 526-538(2008).
38. G.. Shanmugam, S.. Sampath, K. K.. Selvaraj, D. J.. Larsson, B. R.. Ramaswamy, Non-steroidal anti-inflammatory drugs in Indian rivers, Environ. Sci. and Pollut. Res., 21(2), 921-931(2014).
39. P.. Paíga, L. H.. Santos, S.. Ramos, S.. Jorge, J. G.. Silva, C.. Delerue-Matos, Presence of pharmaceuticals in the Lis river (Portugal): Sources, fate and seasonal variation, Sci. Total Environ., 573, 164-177(2016).
40. K.. Komori, Y.. Suzuki, M.. Minamiyama, A.. Harada, Occurrence of selected pharmaceuticals in river water in Japan and assessment of their environmental risk, Environ. Monitoring and Assess., 185(6), 4529-4536(2013).
41. W.. Li, L.. Gao, Y.. Shi, J.. Liu, Y.. Cai, Occurrence, distribution and risks of antibiotics in urban surface water in Beijing, China, Environ. Sci.: Proc. & Impacts., 17(9), 1611-1619(2015).
42. L.. Patrolecco, N.. Ademollo, P.. Grenni, A.. Tolomei, A. B.. Caracciolo, S.. Capri, Simultaneous determination of human pharmaceuticals in water samples by solid phase extraction and HPLC with UV-fluorescence detection, Microchem. J., 107, 165-171(2013).
43. S. H.. Lee, H. W.. Jung, J. Y.. Jung, H. J.. Min, B. R.. Kim, S. G.. Park, J. E.. Oh, Characteristics of Occurrence of Pharmaceuticals in the Nakdong River, J. Environ. Sci. Int., 35(1), 45-56(2013).
45. Nakdong River Basin Environmental Office, A Survey on the Monitoring of Potentially Hazardous Compounds and Contamination Routes in Tributary of the Nakdong River Systempp. 1~212(2015).
46. Nakdong River Basin Environmental Office, Water Quality and Discharge Monitering of Tributaries in the Nakdong River Systempp. 1~465(2015).
47. H. Y.. Kim, H. J.. Jung, J. J.. Yoo, T. H.. Lim, Y. K.. Lim, E. O.. Jung, Occurrence of Pesticides in the Nakdong River Basin and Risk Assessment, J. Korean Soc. Environ. Anal., 19(1), 1-11(2016).
48. Daegu Regional Environmental Office, Survey on the Hazardous Substances of the Kumho River Basinpp. 1~207(2015).
49. H. J.. Son, S. H.. Jang, Occurrence of Residual Pharmaceuticals and Fate, Residue and Toxic Effect in Drinking Water Resources, J. Korean Soc. Environ. Eng., 33(6), 453-479(2011).
50. Korea Meteorological Administration Home Page, http://www.kma.go.kr/weather/climate/past_tendays.jsp, March(2017)
51. K.. Choi, Y.. Kim, J.. Park, C. K.. Park, M.. Kim, H. S.. Kim, P.. Kim, Seasonal variations of several pharmaceutical residues in surface water and sewage treatment plants of Han River, Korea, Sci. Total Environ., 405(1), 120-128(2008).
52. S. M.. Bae, Respiratory bacteria and viruses in the aetiology of acute pharyngitis in KoreaPublic Health Weekly Report, KCDC, 5(4), ISSN:2005-811X2012.
53. Health Insurance Review and Assessment Service (HIRA) http://opendata.hira.or.kr/home.do, March(2017)
54. S. W.. Nam, B. I.. Jo, Y.. Yoon, K. D.. Zoh, Occurrence and removal of selected micropollutants in a water treatment plant, Chemosphere., 95, 156-165(2014).
55. P. C.. Lindholm-Lehto, H. S.. Ahkola, J. S.. Knuutinen, S. H.. Herve, Widespread occurrence and seasonal variation of pharmaceuticals in surface waters and municipal wastewater treatment plants in central Finland, Environ. Sci. and Pollut. Res., 23(8), 7985-7997(2016).
56. J. L.. Santos, I.. Aparicio, E.. Alonso, Occurrence and risk assessment of pharmaceutically active compounds in wastewater treatment plants. A case study: Seville city (Spain), Environ. Int., 33(4), 596-601(2007).
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||