|
The Korean text of this paper can be translated into multiple languages on the website of http://jksee.or.kr through Google Translator.
AbstractPlastic pollution is an important issue in the environment. However, there are few systematic studies on the harmful substances that can be leached out from plastics. The objective of this study is to improve a method for monitoring various styrene oligomers (SOs) derived from polystyrene (PS), one of the major plastics. To achieve this goal, in this study, extraction and concentration methods were modified to reduce the analysis time and to improve the convenience of the analysis procedure. In addition, this study selected a more appropriate internal standards (IS) for quantitative monitoring of SOs. Through a series of experiments, Acenaphthene-d10 (Ace-d10) was the most appropriate IS to quantify styrene monomer (SM). Phenanthrene-d10 (Phe-d10) was an appropriate IS for 1,3-diphenyl propane (SD-1), 2,4-diphenyl-1-butene (SD-3), trans-1,2-diphenyl cyclobutane (SD-4), and 2,4,6-triphenyl-1-hexene (ST-1). In addition, 4-Terphenyl-d14 (4-ter-d14) was appropriate as an IS for monitoring 1a-phenyl-4e-(1'-phenylethyl)tetralin (ST-3), 1e-phenyl-4e-(1'-phenylethyl)tetralin (ST-5) and 1,3,5-triphenylcyclohexane-Isomer mix (A Isomer mixture of 1e,3e,5a-triphenylcyclohexane and 1e,3e,5e-triphenylcyclohexane, ST-6mix). Recovery tests were conducted to verify selected ISs, which ranged from 80% to 120%. Then, improved SOs analysis method was applied to the seawater and sand samples of Jeju Island coast to measure SOs. This study is expected to contribute to the assessment of the impact of PS plastic contamination in the environment.
요약플라스틱 오염은 매우 중요한 환경적 이슈이다. 하지만 플라스틱에서 침출 또는 유래될 수 있는 유해물질에 관한 체계적인 연구는 매우 드물다. 이 연구의 목적은 주요 플라스틱의 한 종류인 폴리스타이렌(Polystyrene, PS)에서 유래되는 다양한 스타이렌 올리고머(Styrene Oligomers, SOs)를 환경에서 효과적으로 모니터링하기 위한 방법을 개발하는 것이다. 이를 위해 분석시간 절감과 분석절차의 편의성 증진을 목적으로 추출 및 농축방법을 개선하여 적용하였다. 또한, 다양한 내부표준물질(Internal Standard, IS)을 시험하여, SOs를 정량하는데 가장 적합한 IS를 선정하였다. 실험결과, Styrene monomer (SM)은 Acenaphthene-d10 (Ace-d10)을, 1,3-diphenyl propane (SD-1), 2,4-diphenyl-1-butene (SD-3), trans-1,2-diphenyl cyclobutane (SD-4), 2,4,6-triphenyl-1-hexene (ST-1)은 Phenanthrene-d10 (Phe-d10)을, 1a-phenyl-4e-(1'-phenylethyl)tetralin (ST-3), 1e-phenyl-4e-(1'-phenylethyl)tetralin (ST-5), 1,3,5-triphenylcyclohexane-Isomer mix (A Isomer mixture of 1e,3e,5a-triphenylcyclohexane and 1e,3e,5e-triphenylcyclohexane, ST-6mix)는 4-Terphenyl-d14 (4-ter-d14)을 각각 IS로 선택하여 정량하는 것이 효과적임을 알 수 있었다. 회수율 실험은 선정된 IS 및 실험방법의 검증을 위해 진행되었으며, 측정된 SOs 회수율은 일반적인 회수율 허용범위(80~120%)를 모두 만족하는 것으로 나타났다. 제주도 해안 해수와 해사에 개발된 SOs 분석법을 적용한 결과 PS 플라스틱 오염의 영향을 평가하는데 기여할 것으로 판단된다.
1. 서 론최근 플라스틱 조각으로 인한 환경오염문제가 해외뿐만 아니라 국내에서도 큰 주목을 받고 있다[1~3]. 플라스틱은 가공이 용이하며 가볍고 튼튼하여 그 사용성이 매우 편리하다. 이로 인해 1950년대를 기점으로 플라스틱 생산량은 급격하게 증가하였고, 2017년을 기준으로 지구 전체의 플라스틱 생산량은 약 3억 5천만 톤에 이른 것으로 알려져 있다[4,5]. 또한, 플라스틱을 구성하는 재질이 점차 다양화되어 지금은 그 종류만 약 30여종에 이르며, 현재 우리가 일상에서 흔히 사용하는 제품의 소재로 널리 이용되고 있는 실정이다[4,5].
고분자 재료로써 플라스틱은 물리/화학적으로 안정되고, 생물학적으로도 내성이 있는 매우 안정된 물질로 인식되고 있다[4]. 하지만 이런 특성으로 인해 플라스틱은 환경에서 거의 분해되지 않고 지속적으로 축적되면서 오염을 유발하고 있다[6~8]. 예를 들어, 해양환경으로 유입된 폐플라스틱 조각이 해양생물체에 축적되어 질식, 소화 장애 등을 유발하면서 해양생태계에 악영향을 초래하고 있다[9,10]. 게다가, 비극성을 갖는 플라스틱의 특성으로 인해, 폐플라스틱 조각 표면에 유해한 잔류성유기오염물질(persistent organic pollutants, POPs)이 흡착되어 다른 곳으로 이동함으로써, 환경 내 오염을 확산시키는 매개체로 작용하기도 한다[11,12].
폐플라스틱 조각으로 인한 환경오염은 많은 연구자에 의해 조사되었다. 특히, 해양환경에서 폐플라스틱 조각으로 인한 환경오염의 정도에 관한 연구들은 매우 광범위하게 수행되었다. 이들 연구는 단순히 폐플라스틱 조각을 개수하는 방법에 관한 연구[13], 미세플라스틱 및 나노플라스틱의 농도와 그 축적량에 관한 연구[14], 매개 중심성을 이용한 해양 플라스틱 폐기물의 경로 예측 및 효율적인 수거지점 제안[15], 플라스틱에 첨가된 다양한 화학 첨가제의 모니터링 및 그 위해성을 평가하는 연구 등 다양하다[16,17]. 최근에는 플라스틱 재질 자체에서 침출될 수 있는 화학물질도 관심의 대상이 되고 있다[18,19]. 특히, 침출되는 다양한 화학물질 중에서 스타이렌 올리고머(styrene oligomers, SOs)는 발암 물질로 의심받고 있으며, 매우 안정적인 플라스틱의 특성상 수환경에서도 지속적으로 유해할 것으로 여겨지고 있다[20]. 이런 이유로 SOs에 관한 다양한 모니터링 조사는 연안과 해양환경에서 이루어지고 있다[19,21].
일반적으로 SOs는 스타이렌 기반의 고분자 물질에서 유래될 수 있다. 다시 말하자면, 스타이렌 기반 고분자 소재는 스타이렌 단량체(styrene monomer, SM)의 중합반응(polymerization)을 통해 생성되고, 주로 폴리스타이렌(polystyrene, PS) 플라스틱 재질과 타이어 등 다양한 고무 제품이 이에 해당된다[22]. 특히, PS는 전 세계 사용량 기준으로 6대 플라스틱 중 하나로[19], 주로 식품을 포장하거나 담는 소재, 전자제품 포장재, 절연체 등의 재료로 널리 일상적으로 사용되기도 한다[23]. SOs는 PS 플라스틱 등 스타이렌 기반 고분자 제품을 중합하는 과정에서 부산물(by-products)로 생성되는 인위적 화학물질이다[24]. 그래서 SOs는 지속적으로 환경에 존재할 수 있는 새로운 환경오염물질일 수 있다[19]. 이러한 이유로 과거에는 SOs의 연구가 주로 식품이나 건강 분야에 집중되어 왔고[18], 환경 분야 연구가 되고 있다.
현재 주로 조사되는 SOs는 스타이렌 모너머(Styrene Monomer, SM)을 포함하여 이성질체 4종을 갖는 스타이렌 다이머(styrene dimers, SDs)와 이성질체 7종을 갖는 스타이렌 트리머(styrene trimers, STs)이다[25]. SOs와 관련된 기존의 연구들은 주로 해수와 해양 모래 등 해양환경을 중심으로 보고되었다[19,21,26~28]. 또한 해양환경에서 SOs의 함량을 측정함으로써 PS로 인한 해양환경의 오염수준을 측정하고, 나아가 PS 오염을 정량적으로 평가하기 위한 시도가 있었다[19,21,27~29]. 이들 연구에서 SOs를 정량하는 방법으로 기체크로마토그래피/질량분석기(gas chromatograph/mass spectrophotometer, GC/MS)를 이용한 내부표준법(Internal standard method)을 사용하였다. SOs 시료 전처리 방법을 살펴보면, Hong et al. (2016)은 모래 및 퇴적물 시료의 추출 방법으로 속슬렛(Soxhlet)을 사용하여 분석 항목을 추출하였고[18], Saido et al. (2014)과 Kwon et al. (2014, 2017)은 농축 과정에서 회전식 증발 농축기(Rotary Evaporator)를 사용하여 농축을 진행하였다[21,27~28]. 하지만 속슬렛 추출법의 경우, 추출 시간만 24시간으로 많은 분석시간이 요구되고, 가열에 따른 많은 열에너지를 소비해야 하는 단점이 있으며, 회전증발농축의 경우에는 농축이 진행되는 동안 실험자가 세심한 주의를 기울이며 지속적으로 관찰한다는 점에서 그 편의성이 많이 떨어진다. 또한, 기존 연구에서는 페난트렌(Phenanthrene, PH)을 내부표준물질(Internal Standard, IS)로 주로 사용하였는데[19,21,27~28,30], PH는 원유의 주요 성분으로 수생 생태계에 풍부하게 존재하기 때문에 시료 채취 시 시료에 이 성분이 이미 존재할 가능성이 있다[31]. 그러므로 SOs 분석을 위한 시료전처리 방법의 개선 및 적합한 IS 선정에 대한 연구가 필요하다.
본 연구의 목적은 환경에 존재하는 SOs를 용이하게 모니터링하기 위한 분석법을 개발하는 것이다. 이를 위해 분석시간을 절감하고 분석절차의 편의성 증진을 위하여 추출 및 농축방법을 개선하여 적용하였다. 또한, SOs의 일정한 회수율 확보를 위해 다양한 표준물질들을 IS로 사용하여 평가하였다. 이를 통해 SOs분석에서 가장 적합한 IS를 선정하고, 개발된 SOs 분석법을 실제 해양 시료에 적용하여 적용가능성을 평가하였다.
2. 재료 및 방법2.1. 시약 및 재료SOs 표준물질 중 SM은 Sigma-aldrich (St. Louis, USA)에서, 그 외 나머지 표준물질은 Wako chem. (Tokyo, Japan)에서 구매하였다. 또한, SOs에 따른 적절한 IS를 선정하기 위하여 4가지 표준물질을 준비하였다. 4가지 IS 모두 AccuStandard (New haven, USA)에서 구매하였으며, SOs와 IS 표준물질에 대한 상세한 내용은 Table 1에 나타내었다.
SOs 항목 중 cis-1,2-diphenyl cyclobutane (SD-2), 1a-phenyl-4a-(1'-phenylethyl)tetralin (ST-2), 1e-phenyl-4a-(1'-phenylethyl)tetralin (ST-4)의 경우, 구매 과정상 착오가 있어, 교환 및 재구매에 많은 시간이 소요되어 이 연구의 분석물질에서는 제외하기로 결정하였다.
실험 용매는 디클로메탄(Dichloromethane, DCM) (Merck KGaA, darmstadt, Germany)을, Surrogate로는 비페닐(biphenyl, BP) (Wako Chem., Tokyo, Japan)을 각각 구매하여 사용하였다. GC/MS 분석과 유리 재질의 실험도구를 세척하기 위해 벤젠과 메탄올(Merck KGaA, darmstadt, Germany)이 사용되었고, 이들 용매는 모두 reagent grade 등급이었다. 수분 제거용 Sodium sulfate anhydrous (Na2SO4) 시약은 E.P (Extra Pure, DUKSAN, Ansan, Korea) 등급을 사용하였다.
2.2. 시료채취 위치 및 방법연구에서 사용된 해수와 모래 시료는 제주도 해안지역에서 채취되었으며, Fig. 1에 나타내었다. 김녕 해변(Gimnyeoung Beach, 1)에서 채취한 해수 시료를 W1, 모래 시료를 S1, 함덕 해변(Hamdeok Beach, 2)의 해수 시료를 W2, 모래 시료를 S2, 삼양 해변(Samyang Beach, 3)의 해수 시료를 W3, 모래 시료를 S3으로 각각 표기하였다.
시료의 채취방법은 기존 연구를 참조하여 수행되었다[21,26]. 해수 시료는 해변을 따라 수심 약 40 cm 깊이에서 스테인레스 스틸 재질의 비이커에 채취되었고, 불순물 제거를 위해 cotton plug로 여과한 시료 2 L를 유리 재질의 분별깔때기(Separatory Funnel)로 옮겼다. 이후, DCM 25 mL을 넣고 약 10분간 격렬하게 분별깔때기를 흔들어 추출하였으며, 이 과정을 4회 반복하여 총 100 mL의 DCM 용액을 최종 수집하였다.
모래 시료는 해변의 표면에 존재하는 모래 약 100 g을 채취하였다. 이후 시료를 잘 혼합하여 유리 용기에 보관한 후 실험실로 옮겨 실험을 진행하였다. 특히, 시료의 채취와 추출 과정에서 불필요한 오차를 없애기 위해 플라스틱 재질이 포함된 실험기구와 장비는 사용하지 않았다.
2.3. 회수율 및 내부표준물질 평가 시료의 조제내부표준물질(IS) 평가 실험 시료는 실험실 조건에서 탈염수에 SOs 표준물질과 BP를 혼합한 용액(1 mg/L) 30 µL을 spiking하여 조제하였다. 탈염수(>18 MΩ cm)는 초순수 제조기(Model: Power Max, Human Science, Hanam, south Korea)로 즉시 제조한 것을 사용하였다. 회수율 실험 시료는 실험실 조건에서 인공 모래와 인공 해수 두 가지 조건을 설정하여 조제하였다. 먼저 모래는 Wako Chem. (Tokyo, Japan)에서 구매하였으며 벤젠, 메탄올, DCM 순으로 세척하여 실험에 사용하였다. 이후 회화로(Model: AT-E58, Isuzu, Tokyo, Japan)로 300℃에서 6시간 가열하여 미량 잔류하는 모래 내 이물질을 제거하였다[21]. 인공 해수는 물 1 L당 Aquamarins S (Yashima, Sakai, Japan) 40.6 g을 첨가하여 조제하였다[21]. 이후 인공해수, 인공모래 시료에 SOs 표준물질과 BP를 혼합한 용액(1 mg/L) 30 µL을 내부표준물질 평가 시료와 동일하게 spiking하여 준비하였다.
2.4. 전처리 방법회수율 평가 실험 및 IS 평가 실험, 해양 시료 전처리 과정은 기존 연구 방법을 참고하여 진행하였다[18,21]. 해수 및 IS 평가 실험 시료는 추출과정을 총 4회 반복하여 얻은 DCM 100 mL에 BP (1 mg/L) 30 µL를 주입한 후 교반하여 여과 후, 질소농축기(model: Turbovap classic Ⅱ, uppsala, sweden)를 사용하여 약 0.75 mL가 될 때까지 농축을 진행하고, 여기에 IS (2 mg/L) 30 µL를 주입하여 분석시료로 하고 GC/MS로 분석하였다.
모래 시료의 경우, 5.0 g을 정밀히 달아 분취한 후 BP (1 mg/L) 30 µL을 주입하였다. 이후 DCM 25 mL를 넣고 초음파추출기(model: Sonifier 450, Branson Ultrasonics Corp., Danbury, USA)로 1분간 4회 반복 추출하여 총 100 mL로 하였다. 이후 농축 및 분석과정은 해수 시료와 동일하다.
2.5. GC/MS 분석방법 및 QA/QC시료분석은 기체크로마토그래피(HP 7820A) - 질량분석기(HP 5977B)를 사용하였다. 사용 컬럼은 HP-5 MS capillary column (30 m×250 µm×0.25 µm, Agilent, Santa Clara, USA)이고, MS (mass spectrometry)는 전자 이온화 모드에서 70 eV로 작동되었다. 인젝터는 splitless mode로 1 µL을 주입하고 온도는 280℃로 유지하였다. 헬륨을 Carrier gas로 사용했으며 유량은 1.4 mL/min으로 일정하게 유지하였다. 오븐 온도는 먼저 50℃에서 2분간 대기하고, 분당 8℃씩 상승시켜 258℃까지 도달시킨다. 이후 분당 4℃씩 290℃까지 증가시키고 이를 4분간 유지하며, 총 run time은 40분으로 설정하였다. MSD transfer line의 온도는 290℃, MS source 온도는 300℃로 각각 유지하였다. 분석은 SIM mode로 분석하였고, SOs와 내부표준물질에 대한 선택이온(Selected ion)은 Table 1에 나타내었다.
각 SOs 항목의 검출한계는 약 2 µg/L 이하이고, 이는 신호 대 잡음비(signal-to-noise ratio)의 3배에 해당하는 값으로 결정되었다. 또한, 정도 보증을 위해 회수율 평가를 실시하여 분석방법을 검증하였으며, 회수율 실험 시료 및 해양 시료의 SOs 정량에는 IS 평가 실험 결과를 기반으로 선정한 내부표준물질을 바탕으로 내부표준법을 사용하여 정량하였다.
3. 결과 및 고찰3.1. 내부표준물질(IS) 선정본 연구는 SOs를 정량적으로 분석하는 과정에서 가장 적합한 IS를 선정하기 위하여 실시하였다. 실험에 사용한 표준물질은 모두 동위원소로 치환된(Isotopically-labeled) 물질만을 고려하였다(Table 1).
IS로 사용 가능한 물질의 조건은 보편적으로 GC/MS에서 머무름 시간이 분석대상물질과 가까울수록 좋으며, 피크가 다른 성분들과 서로 중첩되지 않아야 한다[32]. 그래서 IS 선정을 위해 Fig. 2에 나타난 SOs와 IS 사이의 머무름 시간의 상관관계와 Table 2에 제시된 평균회수율 및 RSD (Relative Standard Deviation) 결과를 종합적으로 고려하였다.
먼저, SM과 BP는 IS로 Ace-d10를, SD-2, SD-4, ST-1은 Phe-d10를 사용할 경우 회수율과 RSD 결과가 가장 좋았으며 머무름 시간도 다른 IS보다 비교적 가깝기에 각 항목의 IS로 선정하였다. SD-1의 경우에는, Ace-d10에서 가장 높은 회수율을 보였지만, Phe-d10의 머무름 시간이 SD-1와 더 가까우며, 회수율 또한 94%로 높게 나타나, SD-1을 정량하는 IS로는 Phe-d10을 선정하였다. 이와 동일한 이유로 ST-3, ST-5, ST-6mix 역시 Phe-d10보다 머무름 시간이 더 가까운 4-ter-d14를 IS로 선정하였다.
이 실험결과를 통하여 여러 가지 항목을 동시에 분석하여 정량할 경우, 하나의 특정 IS만을 선정하여 정량을 진행하기보다 각각 항목에 대응하는 IS를 선정하여 분석하는 것이 보다 더 정확한 결과를 얻는데 도움을 줄 수 있을 것이라 판단된다.
3.2. 회수율 실험회수율 실험은 개선된 실험 방법과 앞서 실시한 IS 실험 결과에 대한 검증 및 해양 시료 분석 결과에 대한 신뢰성 확보를 위해 실시하였다. 실험실에서 임의로 인공 해수와 인공 모래 시료를 사용하였으며 총 4회 반복으로 진행하였다. 모래 시료의 추출 방법으로는 속슬렛 대신 초음파 추출(Ultrasonic-assisted extraction)을 사용하여 실험시간을 현저히 단축시켰으며, 농축 방법으로는 센서가 부착된 농축기를 사용하여 실험의 편의성을 증가시켰다. GC/MS 분석 전 주입한 IS로는 IS 평가 실험 결과를 바탕으로 선정한 3가지 IS (Ace-d10, Phe-d10, 4-ter-d14)를 사용하였고, 내부표준법을 통하여 해당 SOs를 정량하여 결과를 산출하였다.
인공 해수와 모래 시료에 대한 SOs 회수율 결과를 Table 3에 나타내었다. 회수율의 경우, 해양 모래와 해수 모두 SD-1, ST-5 두 물질의 회수율이 다른 항목에 비하여 비교적 낮게 측정되었지만, 일반적인 회수율 허용범위(80~120%)에는 모두 만족하였다. 또한 SD-1, ST-5를 제외한 나머지 항목들은 모두 90%를 초과하는 높은 회수율을 보였다. SOs 총 항목에 대한 회수율 평균값은 모래시료가 92% 해수시료가 91%로, 모래시료의 회수율이 아주 근소한 차이로 높게 측정되었다. RSD (%)의 경우, 해양 모래에서 ST-1이 11%로 근소하게 높은 것을 제외하고, 나머지 항목에서는 해양 모래와 해수 모두 6% 미만으로 결과 값의 변동이 적고 실험의 높은 재현성이 확인되었다.
회수율 결과를 이전 연구와 비교해 보면, Hong et al. (2016)에서 총 SOs 평균 회수율은 92%로 이 연구의 실험결과와 매우 유사하게 나타났으며, Saido et al. (2014)의 연구에서는 총 SOs 평균 회수율이 해수에서 94% , 모래에서 96.5%로 본 연구의 회수율 결과보다 근소하게 높았지만 유의미한 차이가 난다고 할 수 없었다. 따라서 SOs 분석을 위해 새로 개발한 분석법이 객관적인 신뢰성과 타당성이 있음을 검증하였다.
3.3. 제주도 해안의 SOs 농도개선된 SOs 분석법을 적용하여 실제 해양 시료의 SOs 농도를 평가해 보았다. 시료는 제주도 해안의 해수와 모래를 각각 3점씩 채취하여 진행하였으며, 실험실에서의 처리 및 분석방법은 회수율 실험과 동일하게 적용하였다.
Fig. 3은 해양 모래 시료와 해수 시료의 평균 SOs 농도를 나타낸 그래프이다. 해양 모래 시료의 경우 SOs의 총 농도는 S1, S2, S3 차례대로 각각 4.391 µg/L, 3.617 µg/L, 8.889 µg/L로 측정되었으며, SM, SD, ST의 함량비율은 S1 (SM: 37%, SD: 9%, ST: 54%), S2 (SM: 26.5%, SD: 36%, ST: 37.5%), S3 (SM: 35.7%, SD: 9.5%, ST: 54.8%)이다. 해수 시료의 경우 SOs의 총 농도가 W1, W2, W3 각각 0.017 µg/L, 0.019 µg/L, 0.020 µg/L으로 매우 낮은 농도를 보였다. SM, SD, ST 함량비율은 W1 (SM: 47%, SD: 6%, ST: 47%), W2 (SM: 70%, SD: 16%, ST: 14%), W3 (SM: 34.7%, SD: 12.5%, ST: 52.8%)로 나타났다. 모래시료의 BP 회수율은 S1= 94.1%, S2= 93.5%, S3= 94.1%이며, 수질시료는 W1= 99.8%, W2= 95.4%, W3= 91.53%로 평균 약 95%의 높은 회수율을 보여, 분석 방법에 대한 신뢰성을 검증하였다.
실험 결과, 해양 모래 시료가 해수 시료보다 SOs 농도가 훨씬 높은 것으로 확인되었으며, S2, W2 두 시료를 제외한 나머지 시료에서 SM:SD:ST 함량비율이 거의 유사하게 측정됨을 알 수 있었다. W2 시료의 경우 S2와 비교하였을 때 SM의 함량만이 특징적으로 더 높은 경향을 보여 시료 채취 및 분석 도중 오염에 대한 가능성이 있으나, 매우 미량만이 검출되었기에 오염여부는 확실하지 않다. 해양 모래가 해수 내 SOs 농도보다 더 높은 경향을 보이는 결과는, 전 세계적으로 조사된 결과에서 해수보다 해양 모래가 더 높은 농도를 보이기 때문이다(모래: 3679±8199.2 µg/L, 해수: 5.1±6.4 µg/L) [18].
북태평양 서쪽 해양의 SOs 오염에 대한 이전 연구사례를 살펴보면, 총 SOs 농도가 한국(모래: 57.9 µg/L, 해수: 5.9 µg/L), 일본 혼슈(모래: 335.3 µg/L, 해수: 4.7 µg/L), 일본 훗가이도(모래: 100.0 µg/L, 해수: 4.8 µg/L) 등으로 본 연구 시료보다 높게 보고되었다[18]. 분석시료 내 SOs 항목별 분포비율은 ST>SM>SD 순으로 비교적 경향이 뚜렷하게 나타났으나, 연구 사례에서 SOs 항목의 해양 분포 비율은 ST>SD (or ST)>SM 순 이었다[18,26]. ST가 가장 많은 기여를 하는 것은 유사하였으나, SD와 SM의 기여도 부분은 상이하였다. 이전 연구사례에 비해 시료 농도와 SOs 항목별 분포 비율이 차이를 보이는 것은, 분석시료 수가 3점으로 비교적 적고 농도 또한 미량이었기 때문에 정확한 비교가 어려울 것으로 생각된다. 따라서 추가지점 모니터링과 같은 연구가 더 필요할 것으로 판단된다.
4. 결 론해양환경에 존재하는 SOs 모니터링을 위한 효과적인 분석법을 개선 및 개발하고자 하였다. 이를 위해 다양한 내부표준물질(IS)을 선정한 후, GC/MS로 분석한 결과를 평가하여 시료 내 SOs 분석에 가장 적합한 IS를 선정하였다.
IS 평가 실험 결과, Styrene monomer (SM)은 Acenaphthene-d10 (Ace-d10)을, 1,3-diphenyl propane (SD-1), 2,4-diphenyl-1-butene (SD-3), trans-1,2-diphenyl cyclobutane (SD-4), 2,4,6-triphenyl-1-hexene (ST-1)은 Phenanthrene-d10 (Phe-d10)을, 1a-phenyl-4e-(1'-phenylethyl)tetralin (ST-3), 1e-phenyl-4e-(1'-phenylethyl)tetralin (ST-5), 1,3,5-triphenylcyclohexane-Isomer mix (A Isomer mixture of 1e,3e,5a-triphenylcyclohexane and 1e,3e,5e-triphenylcyclohexane, ST-6mix)는 4-Terphenyl-d14(4-ter-d14)을 각각 IS로 선택하여 정량하는 것이 가장 적합하였다. 회수율 실험은 선정된 IS와 개선된 실험 방법의 유효성을 검증하기 위해 실시되었으며, SOs 총 항목에 대한 회수율 평균값은 모래시료가 92%, 해수시료가 91%로 통상적인 회수율 적정 범위인 80~120%를 만족하였다. 개발된 SOs 분석법을 통한 제주도 해안 3지점의 해수와 해사의 SOs 농도 측정 환경에서 PS 플라스틱 오염의 영향을 평가 할 수 있음을 확인하였다.
Acknowledgments이 논문은 2019년도 정부(교육부)의 재원으로 한국연구재단의 지원을 받아 수행된 기초연구사업입니다(No. NRF-2017R1D1A1B03027845).
Fig. 1.Map showing the sampling sites of sea water and sea sand of Jeju Special Self-Governing Province. 
Fig. 2.SIM mode chromatogram derived from styrene oligomers and newly selected internal standards with retention time. (*: Internal Standard) 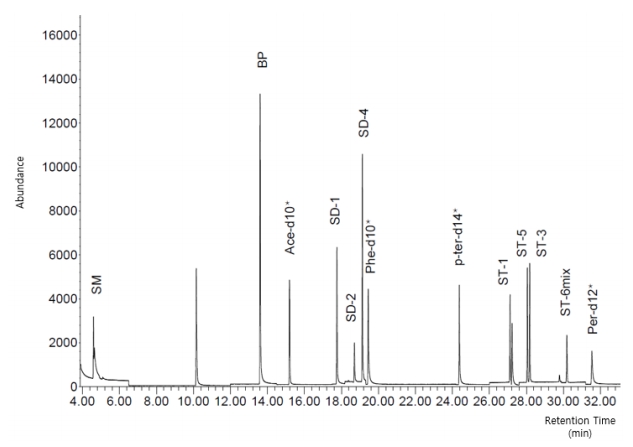
Fig. 3.The concentration of Styrene Oligomers (SOs) in sea-sand and sea-water samples of Jeju Special Self-Governing Province. (SM: Styrene Monomer, SD: Sum of SD-1, SD-2, SD-4, STs: Sum of ST-1, ST-3, ST-5, ST-6mix) 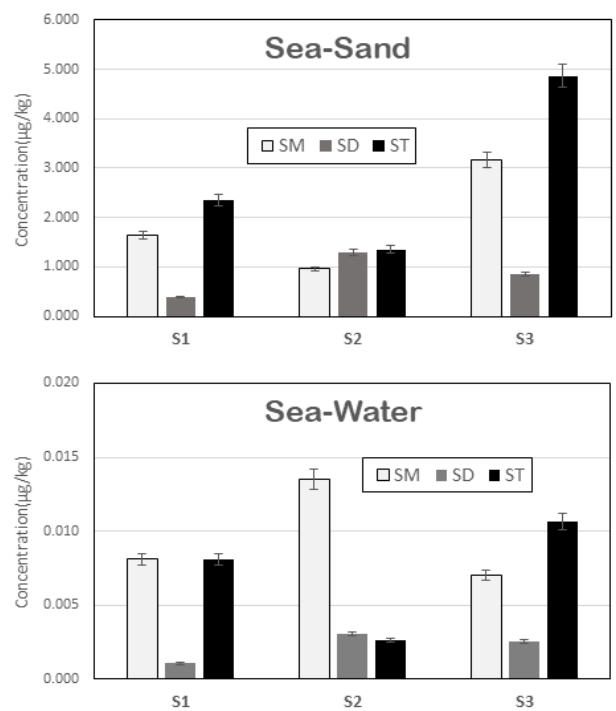
Table 1.Properties of styrene oligomers and Internal standard
Table 2.Result of Internal Standard test References1. R. C.. Thompson, Y.. Olsen, R. P.. Mitchell, A.. Davis, S. J.. Rowland, D.. John, A. F.. McGonigle and Russell, Lost at sea: Where is all the plastics?, Science., 304, 838(2004).
2. C. J.. Moore, Synthetic polymers in the marine environment: A rapidly increasing, long-term threat, Environ. Res., 108(2), 131-139(2008).
3. D. H.. An, J. G.. Kim, Proposing policy for the prevention of marine pollution from microplastics, Journal of environmental policy and administration., 26(3), 77-102(2018).
6. A-G.. Stephanie, D. O.. Patrick, Northern fulmars as biological monitors of trends of plastic pollution in the eastern North Pacific, Mar. Pollut. Bull., 64(9), 1776-1781(2012).
7. M.. Thiel, I. A.. Hinojosa, L.. Miranda, J. F.. Pantoja, M. M.. Rivadeneira, N.. Vásquez, Anthropogenic marine debris in the coastal environment: A multi-year comparison between coastal waters and local shores, Mar. Pollut. Bull., 71(1-2), 307-316(2013).
8. A.. Bakir, S. J.. Rowland, R. C.. Thompson, Enhanced desorption of persistent organic pollutants from microplastics under simulated physiological conditions, Environ. Pollut., 185, 16-23(2014).
9. J. G. B.. Derraik, The pollution of the marine environment by plastic debris: a review, Mar. Pollut. Bull., 44(9), 842-852(2002).
10. D. W.. Laist, Overview of the biological effects of lost and discarded plastic debris in the marine environment, Mar. Pollut. Bull., 18(6), 319-326(1987).
11. A. A.. Koelmans, E.. Besseling, A.. Wegner, E. M.. Foekema, Plastic as a carrier of POPs to aquatic organisms: a model analysis, Environ Sci Technol., 47(14), 7812-7820(2013).
12. R. E.. Engler, The complex interaction between marine debris and toxic chemicals in the ocean, Environ. Sci. Technol., 46(22), 12302-12315(2012).
13. P. G.. Ryan, A simple technique for counting marine debris at sea reveals steep litter gradients between the Straits of Malacca and the Bay of Bengal, Mar. Pollut. Bull., 69(1-2), 128-136(2013).
14. A. L.. Andrady, Microplastics in the marine environment, Mar. Pollut. Bull., 62(8), 1596-1605(2011).
15. Y. S.. Jeon, M. J.. Hong, M. K.. Park, Y. S.. Choi, Path prediction and suggestion of efficient collection points for marine plastic debris based on betweenness centrality analysis, J. Korean Soc. Environ. Eng., 37(7), 426-431(2015).
16. L.. Hermabessiere, A.. Dehaut, P. P.. Ika, C.. Lacroix, R.. Jezequel, P.. Soudant, G.. Duflos, Occurrence and effects of plastic additives on marine environments and organisms: A review, Chemosphere., 182, 781-793(2017).
17. A. A.. Koelmans, E.. Besseling, E. M.. Foekema, Leaching of plastic additives to marine organisms, Environ. Pollut., 187, 49-54(2014).
18. S. J.. Hong, J. H.. Lee, C. K.. Lee, S. J.. Yoon, S. Y.. Jeon, B. O.. Kwon, J. H.. Lee, P. G.. John, J. S.. Khim, Are styrene oligomers in coastal sediments of an industrial area aryl hydrocarbon-receptor against?, Environ. Pollut., 213, 913-921(2016).
19. B. G.. Kwon, K.. Koizumi, S. Y.. Chung, K.. Yoichi, J. O.. Kim, K.. Saido, Global styrene oligomers monitoring as new chemical contamination from polystyrene plastic marine pollution, J. Hazard., 300, 359-367(2015).
20. M.. Kogevinas, W. M.. Gwinn, D.. Kriebel, D. H.. Phillips, M.. Sim, S. J.. Bertke, G. M.. Calaf, C.. Colosio, J. M.. Fritz, S.. Fukushima, K.. Hemminki, A. A.. Jensen, H.. Kolstad, J.. Mráz, S.. Nesnow, L. A.. Nylander-French, M. E.. Parent, M.. Sandy, S. L.. Smith-Roe, G.. Stoner, T.. Suzuki, J. P.. Teixeira, P.. Vodicka, R.. Tornero-Velez, K. Z.. Guyton, Y.. Grosse, F.. El Ghissassi, V.. Bouvard, L.. Benbrahim-Tallaa, N.. Guha, N.. Vilahur, T.. Driscoll, A.. Hall, D.. Middleton, C.. Jaillet, H.. Mattock, K.. Straif, Carcinogenicity of quinoline, styrene, and styrene-7,8-oxide, Lancet. Oncol., 19(6), 728-729(2018).
21. B. G.. Kwon, K.. Saido, K.. Koizumi, H.. Sato, N.. Ogawa, S. Y.. Chung, T.. Kusui, Y.. Kodera, K.. Kogure, Regional distribution of styrene analogues generated from polystyrene degradation along the coastlines of the North-East Pacific Ocean and Hawaii, Environ. Pollut., 188, 45-49(2014).
22. A.. Tossavainen, Styrene use and occupational exposure in the plastics industry, Scand. J. Work, Environ. Health., 4, 7-13(1978).
23. M.. Rani, W. J.. Shim, G. M.. Han, M.. Jang, Y. K.. Song, S. H.. Hong, Hexabromocyclododecane in polystyrene based consumer products: An evidence of unregulated use, Chemosphere., 110, 111-119(2014).
24. P. H. H.. Araújo, C.. Sayer, R.. Giudici, J. G. R.. Poço, Techniques for reducing residual monomer content in polymers: A review, Polym. Eng. Sci., 42(7), 1442-1468(2002).
25. K. I.. Ohyama, F.. Nagai, Y.. Tsuchiya, Certain styrene oligomers have proliferative activity on MCF-7 human breast tumor cells and binding affinity for human estrogen receptor, Environ. Health Perspect., 109(7), 699-703(2001).
26. M.. Eriksen, N.. Maximenko, M.. Thiel, A.. Cummins, G.. Lattin, S.. Wilson, J.. Hafner, A.. Zellers, S.. Rifman, Plastic pollution in the South Pacific subtropical gyre, Mar. Pollut. Bull., 68(1-2), 71-76(2013).
27. K.. Saido, K.. Koizumi, H.. Sato, N.. Ogawa, B. G.. Kwon, S. Y.. Chung, T.. Kusui, M.. Nishimura, Y.. Kodera, New analytical method for the determination of styrene oligomers formed from polystyrene decomposition and its application at the coastlines of the North-West Pacific Ocean, Sci. Total Environ., 473-474490-495(2014).
28. B. G.. Kwon, K.. Amamiya, H.. Sato, S. Y.. Chung, Y.. Kodera, S. K.. Kim, E. J.. Lee, K.. Saido, Monitoring of styrene oligomers as indicators of polystyrene plastic pollution in the North-West Pacific Ocean, Chemosphere., 180, 500-505(2017).
29. B. G.. Kwon, Monitoring of Styrene Oligomers Leached from Polystyrene in the Aqueous Phase, Journal of Chosun College of Science and Technology., 52, 18-24(2017).
30. B. G.. Kwon, S. Y.. Chung, S. S.. Park, K.. Saido, Qualitative assessment to determine internal and external factors influencing the origin of styrene oligomers pollution by polystyrene plastic in coastal marine environments, Environ. Pollut., 234, 167-173(2018).
31. M. L.. Hannam, S. D.. Bamber, T. S.. Galloway, A. J.. Moody, M. B.. Jones, Effects of the model PAH phenanthrene on immune function and oxidative stress in the haemolymph of the temperate scallop Pecten maximus, Chemosphere., 78(7), 779-784(2010).
32. C. K.. Kim, S. W.. Eom, H. K.. Kil, M. H.. Lee, Comparison of Calibration Methods using External Standards and Internal Standards, Journal of the Korean Society for Environmental Analysis., 12(4), 307-313(2009).
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||