1. 서 론
기후변화에 따른 기온상승과 극한 강우사상 발생 증가는 수계내 이상 수질을 빈번하게 발생시키고 있으며, 주요 수계에서 계절에 관계없이 조류에서 기인된 이․취미 유발 물질이 발생되고 있다[1,2]. 또한, 먹는물에 대한 소비자의 기대심리가 높아져 기존 수질기준 이상의 품질이 요구되고 있어, 이에 환경부는 먹는물 수질기준 이외에 맛․냄새 유발물질인 geosmin과 2-MIB가 포함된 27개 항목의 감시항목을 설정하여 모니터링하고 있다.
맛․냄새 유발물질인 geosmin, 2-MIB의 제거를 위한 국내 고도처리공정은 주로 산화공정과 활성탄 흡착공정을 조합하여 적용하고 있으며, 흡착공정과 산화공정을 동시에 적용하기 때문에 과도한 운영비 및 시설비가 투입되고 있다. 또한 활성탄 재생 시에는 900~1,000℃의 고온 조건이 필요하므로 이에 따른 운영비 증대 문제 등이 나타나고 있어, 이러한 기존 공정의 한계를 극복할 수 있는 새로운 고도처리공정 필요성이 대두되고 있다[3].
기존 공정의 한계를 극복하기 위해 활성탄을 개질하여 고기능성 및 선택성이 우수한 활성탄을 개발하거나, 신규 흡착 소재개발을 통해 이온교환수지, 탄소나노튜브, 메조공극물질, 그래핀 등이 개발되고 있다[4]. 이러한 신규 흡착제 중 메조공극 기반의 흡착제의 경우 높은 표면적, 우수한 공극구조 등으로 인해 다양한 적용이 이뤄지고 있으며, 메조공극의 특성으로 흡착속도를 기존 활성탄에 비해 크게 증대시킬 수 있다[5,6]. 본 연구에서는 팽창성(swell) 유기실리카 기반의 메조공극 흡착물질이 여과모래에 코팅된 흡착제(Meso-Porous Adsorbent, MPA)를 적용하였다. 본 흡착제는 빠른 흡착속도 이외에 일반 유기물은 흡착하지 않고 소수성 물질만 선택적으로 흡착할 수 있어 상대적으로 낮은 100℃ 온도 조건에서 수회 재생이 가능한 특징을 가지고 있다[7].
신규 흡착물질에 대한 소재연구는 활발히 이뤄지고 있으나, 신규 흡착제를 현장에 적용하기 위한 기초 성능평가 및 설계인자 도출 등 에 대한 연구는 미흡한 실정이다. 따라서 본 연구에서는 신규흡착물질 중 메조공극 팽창성 유기실리카 기반의 흡착제(MPA)를 이용해 흡착제의 기본 흡착성능을 규명하기 위한 등온흡착 평가와 동역학적 평가를 수행하였다.
2. 연구방법
2.1. 실험재료 및 분석
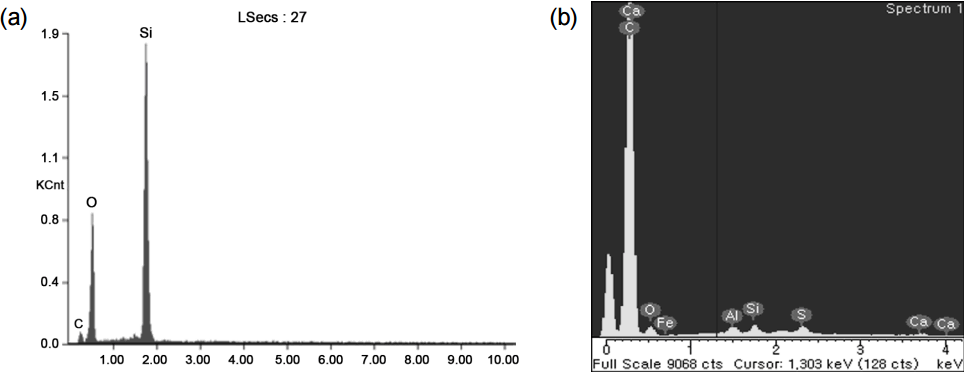
본 실험에 사용한 메조공극 흡착제(MPA)는 흡착성능이 우수한 팽창성 메조공극 유기실리카 물질을 모래에 코팅시킨 제품이며(ABSMaterial, 미국), 본 흡착제와 비교 평가를 위해 Norit GAC 1240모델의 입상활성탄(GAC)을 선정하여 적용하였다. 본 실험을 통해 MPA의 GAC 대체 가능성을 확인하고자 두 흡착제 모두 입경 조절 없이 실험을 수행하였다. 실험에 적용한 MPA와 GAC에 대한 특성은 Table 1에 나타내었으며, Fig. 1에 각각의 흡착제에 대한 Field Emission Scanning Electron Microscopy (FE-SEM; LEO SUPRA 55, Carl Zeiss, Germany) 측정 결과를 나타내었다. Fig. 1의 SEM 측정결과에서 나타나듯이 GAC 표면은 다양한 입자들이 부착되어 있고 또한 거친 표면특성이 나타난 반면, MPA는 표면이 매우 매끄럽고 표면에 부착된 입자가 거의 없는 것으로 평가되었다. 그리고 Table 1에서 제시된 BET Surface area and Pore size Analyzer (BET; Belsorp Max, Bel Japan Inc.) 평가 결과 GAC에 비해 MPA의 표면적이 2,000배 이상 작은 것을 확인 할 수 있었다. MPA의 표면적이 작은 이유는 현장 적용성을 증대시키기 위해 일반 여과모래 표면에 메조공극 유기실리카 물질을 코팅하여 사용하였기 때문이며, 또한 MPA는 팽창성 유기실리카 물질로 코팅되어 있어 오염물과 접촉 시 팽창이 이뤄져 추가적인 공극을 형성하게 되지만 BET 평가 시에는 팽창된 상태의 MPA의 공극 측정은 불가능하여 비팽창된 MPA의 표면적만 측정된 것으로 판단되었다. 그리고 Energy Dispersive X-ray Spectrometer(EDS; GENESIS 2000, EDAX, USA: Linescan of Calcium and Phosphorus)를 이용한 각 흡착제의 원소조성 분석결과 GAC는 탄소, 산소, 알루미늄, 실리카 등 다양한 물질로 구성된 반면, MPA는 주로 실리카, 산소, 그리고 탄소가 주성분으로 구성되어 있음을 확인할 수 있었다.
본 실험에 사용한 오염물은 상수원수 내 대표적인 맛․냄새 유발물질인 geosmin (Wako, Japan)을 메탄올에 용해시켜 Stock 용액을 만들어 초순수(De-ionized distilled water)에 일정량을 주입하여 실험하였다. Geosmin 분석은 GC-MS (Gas chromatography-Mass spectrometry, GC : Agilent technologies 7890A, MS : Agilent technologies 5975C)기기를 사용하였으며, 분석조건은 위의 Table 2에 나타내었다. 실험에서 사용한 geosmin의 농도가 미량이므로 SPME (Solid Phase Micro Extraction)으로 전처리를 진행하였다.
2.2. 실험방법
2.2.1. 등온흡착 실험
등온흡착 실험은 950 mL 갈색병에 서로 다른 농도의 geosmin이 용해된 950 mL 용액에 0.1 g의 MPA와 0.05 g의 GAC를 각각 주입하였다. pH는 7로 조절하였으며, 흡착제 주입 후 교반기를 이용하여 교반강도 150 rpm에서 24 hr동안 흡착반응을 진행하였다. 모든 실험에서 25 ± 1℃ 온도를 유지하였다. 흡착반응 완료 후 샘플을 채취하여 0.45 μm PVDF syringe filter를 이용하여 여과 후 GC-M/S를 이용해 분석하였다.
본 실험을 통해 얻어진 데이터를 이용하여 MPA의 흡착특성을 평가하기 위해 초기 geosmin 농도는 1~80 μg/L 범위에서 흡착실험을 수행하여 Langmuir식 및 Freundlich식의 등온흡착 모델에 적용하여 평가하였다.
3. 결과 및 고찰
3.1. 등온흡착 특성
상수원수 내 대표적인 맛․냄새 유발물질인 geosmin은 소수성 물질(log Kow 3.57)로 고체상에 흡착하려는 경향이 강하고, 고체상에 유기물의 함량이 증가할수록 흡착 경향은 더 강해지게 된다[8,9]. 이러한 각 흡착제에 따른 geosmin의 흡착 특성에 대한 평가 및 특성 정보를 얻기 위하여 등온 흡착실험을 수행하였고 얻어진 결과는 평형상태에서의 geosmin의 농도(μg/L) 변화에 따른 흡착량(μg/g)의 관계로 도시하였다. 일반적으로 평형-흡착식은 Langmuir, Freundlich Isotherms의 두 가지 모델로서 나타내며, Langmuir 식은 흡착제(adsorbent) 표면의 결합자리가 흡착질(adsorbate)과 화학양론 적으로 1 : 1로서 상호 독립적으로 반응하며, 각 반응 자리는 균일한 반응세기를 가진다고 가정하여 만들어진 모델로서 다음과 같이 나타낸다.
여기서 Qe는 평형상태에서 흡착제 단위질량당 흡착된 흡착질의 양(mg/g)이며, Ce는 평형상태에서의 용액 중 흡착질 농도(μg/L), Sm은 평형상태에서 흡착제 단위질량당 흡착된 최대 흡착질의 양(μg/g), KL은 흡착속도와 관련된 Langmuir 상수(L/μg)이다[10].
Freundlich 식은 흡착제의 흡착자리는 균일하지 않으며 흡착량이 증가하면서 흡착 에너지가 연속적으로 감소한다는 가정하에서 만들어진 흡착모델이다. Freundlich 식은 불균질 표면 흡착반응을 하는 액상흡착의 해석에 가장 널리 적용되는 식이다. Freundlich 식은 다음과 같이 나타낼 수 있다.
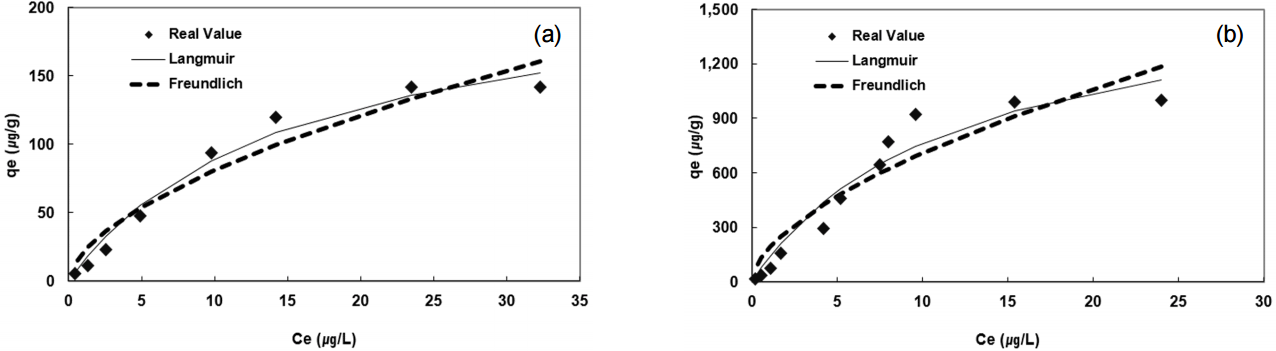
여기서 Qe는 평형상태에서 흡착제 단위질량당 흡착된 흡착질의 양(μg/g)이며, Ce는 평형상태에서의 용액 중 흡착질 농도(μg/L), KF ((μg/g)(L/μg)1/n)는 흡착세기 및 용량과 관련된 Freundlich 등온 흡착상수, 1/n는 흡착자리의 덮힘(surface coverage)에 따른 결합세기의 감소율을 나타내는 흡착상수(i.e., 흡착강도)이다. 일반적으로 KF 값이 높을수록, 그리고 n이 클수록 흡착제 단위무게 당의 흡착량이 높아진다[10]. Langmuir모델과 Freundlich 모델을 이용하여 각각의 흡착제와 geosmin의 흡착관계를 나타낸 결과는 아래 Fig. 3과 4에 나타냈다.
Table 3의 결과와 같이 평형상태에서 MPA와 GAC의 단위질량당 흡착된 geosmin의 실험적 최대 흡착량은 각각 141.57 μg/g, 1,000.85 μg/g으로 평가되었다. 두 흡착제 모두에 대한 등온흡착모델은 실측값과 모델값의 상관계수인 R값 비교결과 Freundlich 모델과 Langmuir 모델의 상관계수가 0.94 이상으로 평가되어 두 모델 모두 실측값을 잘 설명하는 것으로 나타났다.
Langmuir 모델로부터 얻어진 MPA와 GAC에서의 geosmin에 대한 최대 흡착량은 각각 222 μg/g과 1,643 μg/g으로 평가되었으며 흡착속도와 흡착에너지를 나타내는 KL값은 MPA와 GAC가 유사하게 나타났다. Langmuir 방정식의 특징은 아래의 식 (3)과 같은 분리계수 혹은 평형계수로 나타내는 무차원 상수 RL로 표현될 수 있다[11].
여기서, C0는 가장 높은 초기 geosmin의 농도(μg/L)이며 KL은 Langmuir 흡착평형상수이다. RL 0보다 작은 경우 흡착반응은 비가역적이며, 0 < RL < 1일 경우 반응성이 높은 경우로 흡착처리가 적합함을 의미하고 RL이 1보다 큰 경우에는 반응성이 낮으므로 흡착처리가 적합하지 않음을 의미한다. 본 실험을 통해 얻은 MPA와 GAC의 RL은 각각 0.230과 0.126으로 나타나 MPA와 GAC를 이용해 geosmin을 흡착처리 하는 것이 적절한 것으로 평가되었다. 그리고 Freundlich 식으로부터 산정된 흡착능에 대한 척도를 나타내는 KF는 크면 클수록 흡착능력이 우수함을 나타내고, 1/n은 흡착강도를 나타내며 본 값이 0~1 사이에 있으면 흡착이 잘 이뤄지고 2 이상일 경우는 흡착이 불량하다고 알려져 있다[12]. 본 실험을 통해 얻은 MPA와 GAC의 KF는 각각 20.97, 182.35로 GAC가 흡착능력이 더 우수한 것으로 판단되며, 1/n은 모두 0.59를 나타내 두 흡착제 모두 geosmin 흡착에 적합한 것으로 평가되었다.
3.2. 동역학적 흡착 특성
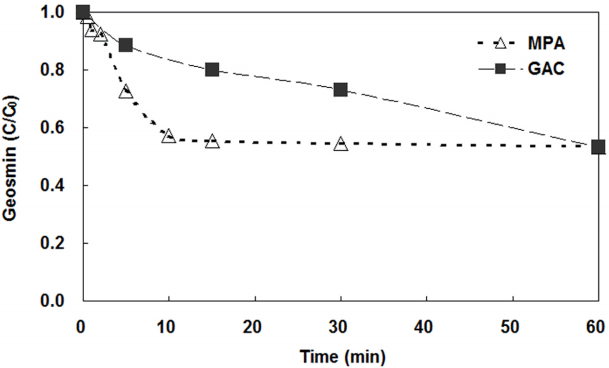
흡착제의 흡착반응 속도 및 반응 완료 시간의 비교를 위해 동력학 실험을 진행하였으며, 시간에 따른 C/C0 결과를 Fig. 4에 나타내었다. 동력학 실험 결과 MPA의 경우 15분 이내에 흡착 반응이 거의 완료되었으며, 본 결과를 통해 GAC 보다 MPA의 흡착반응이 상대적으로 빠른 것으로 판단된다. 결과적으로 대조군인 GAC에 비해 MPA의 흡착반응이 월등히 빠른 것으로 판단되며, 이는 MPA의 공극 및 소재의 특성에 의한 것으로 여겨진다. GAC의 경우 분산에 의해 오염물질이 미세공극으로 들어가 흡착되는데 오랜 시간이 걸리나, MAP는 메조공극형태를 지님으로써 오염물질의 공극으로의 분산이 보다 빠른 특성을 지닌다. 또한 MPA 특유의 공극간 상호연결성으로 인해 빠른 흡착결과를 가져온 것으로 판단된다.
흡착공정에 대한 효율적인 모델을 설계하기 위해서는 동력학적 해석에 대한 이해가 필요하다. 이를 해석하기 위한 흡착반응의 속도에 대한 대표적 모델로써 유사 1차 반응 속도 모델과 유사 2차 반응 속도 모델이 존재한다. 1차 반응 속도식은 Lagergren에 의해 제시되었으며, 수용액상의 용해제로부터 용질의 흡착과정에 널리 적용되는 속도식 중 하나이다. 이 식은 다음과 같다[13,14].
여기서 kad는 유사 1차 반응속도 상수(/min)이며, qe는 평형상태에서 흡착제 단위 g당 흡착된 흡착질의 양(μg/g), qt는 반응시간 t에서 흡착제 표면에서의 흡착량(μg/g), t는 시간(min)이다. 위의 식을 변형시켜 사용할 수 있으며, 그 식은 아래 식 (5)와 (6)으로 나타낼 수 있다.
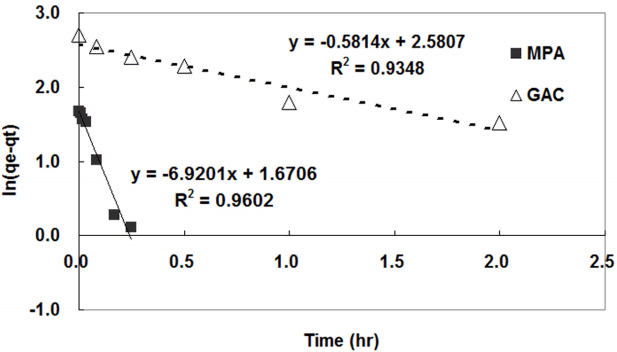
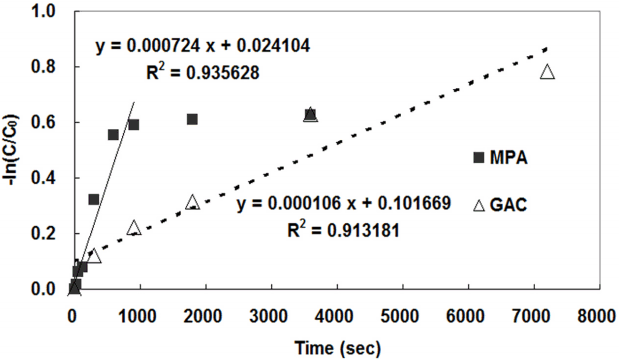
유사 1차 반응속도 모델을 이용하여 흡착속도실험결과를 식 (6)을 적용시켜 Fig. 5에 나타냈으며, 그 결과 MPA가 GAC에 비해 11배 이상 흡착속도가 빠른 것으로 나타났다.
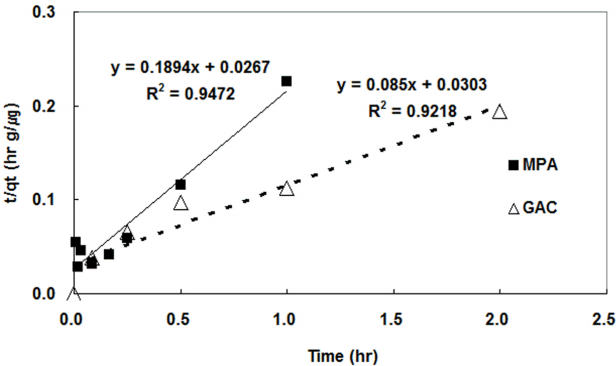
여기서 k2는 유사 2차 반응속도 상수(g/μg․min)이며, qe는 평형상태에서 흡착제 단위 g당 흡착량(μg/g), qt는 반응시간 t에서의 흡착량(μg/g), t는 시간(min)이다. 유사 2차 속도 반응식을 다음 식으로 변형할 수 있으며, 본 식의 기울기와 절편으로부터 k2, qe값을 구할 수 있다[15,16].
유사 1차 반응, 유사 2차 반응 해석을 통한 서로 다른 흡착제들의 반응속도를 구할 수 있었다. 본 실험에서는 유사 1차 반응과 2차 반응 모두 실험값과의 상관성(R)이 0.97이상으로 높게 나타났다. Table 4에서는 GAC는 유사 2차 반응 모델을 적용해 얻어진 이론적 최대 흡착용량과 실험에서 얻어진 최대 흡착용량이 차이를 보이는 반면, Fig. 7에서 나타난 결과와 같이 실험시간 중에서의 흡착 경향은 유사 2차 반응이 더 잘 설명하는 것으로 나타났다. MPA의 경우는 유사1차, 2차 모두 이론적 최대 흡착용량과 실험시간 중의 흡착 경향을 모두 잘 설명하는 것으로 나타났다.
유사 1차 반응해석을 통해 MPA와 GAC의 흡착속도를 비교할 경우 MPA의 흡착속도가 11.4배 높았으며, 유사 2차 반응으로 비교할 경우는 7.3배 더 높은 것으로 나타났다. 따라서 메조공극으로 구성된 MPA가 활성탄에 비해 흡착이 더 빠르게 이뤄지는 것으로 사료된다.
3.3. 흡착제 별 확산 특성
3.3.1. 외부확산 특성
두 흡착제의 흡착특성을 보다 상세하게 규명하기 위해 흡착질의 주된 확산경로를 아래와 같이 확인하였다. 흡착질의 확산경로는 크게 외부확산과 내부 확산으로 나눠진다. 이중 외부 확산 모델은 아래의 식 (9)로 제안된다[17]. 본 식은 식 (10)과 같이 변형하여 적용할 수 있다[18].
여기서 ks는 경막물질이동계수(m2/s)이며, C는 용액중의 흡착질의 농도(μg/L), Cs는 흡착제 표면의 흡착질 농도(μg/g), A는 흡착제의 표면적(m2), V는 용액의 부피(m3), t는 시간(sec)이다.
각 흡착제 별 geosmin의 외부확산모델 적용한 결과는 Fig. 8에 나타낸 것과 같이 MPA의 경우 경막물질이동계수값(ks)이 매우 높아 초기 10분 이내에 흡착반응이 거의 다 이뤄지는 반면 GAC는 상대적으로 낮은 ks값을 나타냈으며 동역학적 평가가 이뤄진 2시간 동안 ks값 변화가 미미한 것으로 나타났다. 이와 같이 MPA의 geosmin에 대한 흡착속도와 평형에 이르는 속도가 GAC에 비해 빠른 이유는 표면특성이 메조공극으로 이뤄져서 물질전달 속도가 빠르며, 또한 소수성 물질에 대해 선택적으로 반응성이 높기 때문에 소수성 특성을 가지고 있는 geosmin과 빠르게 반응하였기 때문으로 사료된다[7]. 또한 유사 1차 혹은 2차 반응상수값과 비교해 MPA의 Ks가 GAC 보다 104배 높은 이유는 MPA의 과소평가된 표면적 분석 결과가 반영되었기 때문으로 판단된다.
3.3.2. 내부확산 특성
내부확산 모델은 Weber와 Morris에 의해 다음과 같이 식 (11)으로 제안되었다.
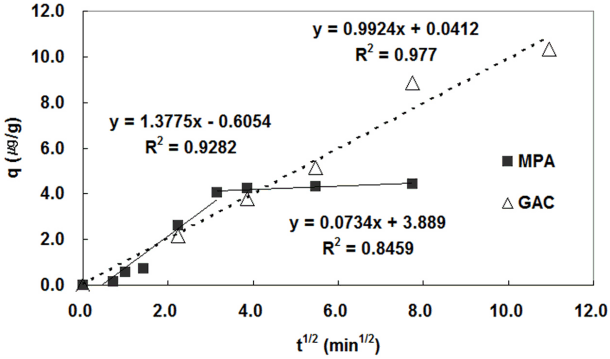
여기서, qt는 시간(t)에서의 흡착량(μg/g), Kid는 세공 내 확산속도상수. t는 시간(min), C는 절편을 나타내는 상수로 경계층의 두께와 관련있다[18]. 여기서 qt대 t1/2로 도시하는 직선의 기울기로부터 Kid를 얻어 흡착제별 내부 확산 특성을 확인할 수 있으며, C값의 경우 값이 증가할수록 경계층의 영향이 커지는 것을 의미한다.
동역학적 흡착실험결과를 내부확산 모델에 적용하여 나타낸 결과는 Fig. 9에 나타냈다. MPA의 경우 초기 10분과 그 이후의 흡착경향이 매우 상이하였으며, 초기 10분에서의 확산속도가 이후보다 19배 이상 빠른 것으로 평가되었다. 이와 같은 결과가 나타나는 이유는 MPA의 빠른 흡착속도로 기인해 초기 10분 만에 흡착평행에 도달했기 때문으로 판단되며, 또한 MPA는 흡착물질을 모래에 코팅하였기 때문에 내부 세공이 존재하지 않은 이유가 복합적으로 작용했기 때문으로 판단된다. 따라서 초기 10분을 경계로 내부확산 속도의 차이가 극명히 나타나는 MPA의 흡착반응은 막확산이 주된 흡착 기작으로 지속적인 내부 확산은 미미한 것으로 사료된다. 반면에 GAC의 경우 흡착속도와 내부 확산속도가 MPA에 비해 상대적으로 느렸으며, 또한 GAC는 표면뿐만 아니라 내부 세공도 잘 발달되었기 때문에 실험시간 동안 일정하게 오염물이 제거되는 것으로 나타났으며 내부 확산속도 역시 실험시간 동안 변화가 미미하게 나타났다.
경계층의 영향을 나타내는 C값의 경우 MPA는 음의 값이 나타났고, GAC는 양의 값이 나타났다. 이는 GAC는 경계층 확산 단계가 존재하는 반면, MPA에서는 경계층의 확산단계가 극도로 축소되어 무시할 만한 수준으로 판단되며, 따라서 경계층에서의 geosmin에 대한 물질전달 속도는 GAC 흡착제에 비해 MPA 흡착제가 더 우수한 것으로 판단된다[19].
4. 결 론
본 연구에서는 메조공극 흡착제 중 하나인 MPA의 적용성 및 흡착특성을 규명하고, 기존 활성탄 공정의 대체 가능성을 평가하고자 흡착제의 특성이 잘 알려진 Norit GAC-1240과 함께 상수원수 내 주요 맛․냄새 유발물질인 geosmin에 대한 등온흡착 및 동역학적 평가를 수행하였으며, 다음과 같은 결론을 얻었다.
1) GAC가 MPA보다 geosmin에 대한 최대 흡착능력이 7배 높은 것으로 평가되었으며, 이런 최대 흡착량 차이는 GAC의 비표면적은 1,103 m2/g인 반면에 MPA는 0.52 m2/g으로 두 흡착제간 비표면적 차이가 나타나기 때문이다. 이러한 비표면적 차이에도 불구하고 흡착량 차이가 7배로 나타난 이유는 MPA가 팽창(swell) 특성이 있어, 오염물을 흡착 후 추가적인 공극 팽창이 이뤄져 흡착 가능 표면적이 증가되었기 때문으로 사료된다.
2) MPA와 GAC의 동역학적 실험 데이터를 유사 1차 및 2차 속도론 모델에 적용하였으며, 두 흡착제는 유사 1차와 2차 속도론 모델 모두를 따르는 것으로 나타났다. MPA 및 GAC의 각각의 1차 속도반응 속도상수(kad)는 6.920 /hr와 0.581 /hr이였으며, 따라서 메조공극으로 구성된 MPA가 GAC에 비해 11배 이상 흡착속도가 빠른 것으로 나타났다.
3) MPA의 경우 주로 외부확산을 통해 흡착이 이뤄지며, 내부 확산에 의한 흡착량은 미미한 것으로 나타났다.
4) MPA를 기존 활성탄을 대신하여 맛․냄새유발 물질제거를 위해 정수장에 적용할 경우, MPA의 빠른 흡착속도 특성에 기인하여 기존 시설에 비해 공상접촉시간(EBCT)을 줄일 수 있다. 또한 활성탄에 비해 총 흡착용량은 7배 낮지만 흡착속도는 11배 높으므로, 짧은 EBCT 조건에서 흡착제가 가지고 있는 흡착용량 전체를 활용 가능할 것으로 판단된다.