소독부산물 전구물질(NOM) 제거를 위한 응집공정의 최적화에 관한 연구
Study of Optimum Coagulation Process for Remove Disinfect By-products Precursor
Article information
Abstract
소독부산물이 전 세계적으로 문제가 제기되면서 보다 신뢰성 있고 효율적인 수처리 공정 기술 개발에 많은 관심이 집중되고 있다. 소독부산물 형성을 줄이기 위한 NOM 제거의 중요성은 증가하고 있다. 응집 공정은 NOM을 용이하게 제거하기 위한 하나의 방법이다. 따라서 본 연구에서는 NOM의 특성과 소독부산물 형성의 관계를 조사하고, 소독부산물의 감소를 위해 NOM의 효율적인 제거를 위한 최적의 응집 조건을 알아내는 것이다. 황산알루미늄과 제2염화철의 최적 응집 조건은 0.15 mM 응집제 주입량에서 pH 5.5로 나타났다. pH 5.5 조건에서 0.15 mM의 제2염화철의 주입한 경우 용존유기탄소는 55% 제거, 트리할로메탄은 65%, 할로아세틱애시드는 67% 감소하였다. 황산알루미늄의 경우 용존유기탄소는 46.3%, 트리할로메탄은 61%, 할로아세틱애시드는 49% 감소하였다. 원수의 pH가 낮을수록 응집공정에 의해 NOM의 제거는 증가하였고 소독부산물 생성은 감소하였다. 또한 제2염화철이 황산알루미늄보다 NOM을 제거하고, DBPs 생성을 감소시키는데 더 효과적이었다.
Trans Abstract
As the problems of disinfect by-products (DBPs) around the world become an issue, much attention has been focused on developing more reliable and efficient water treatment processing technologies. The removal of NOM to reduce the formation of DBPs is increasingly important. Facilitating the removal of NOM is one of the key reasons for using coagulation. Therefore, the objective of this study was to investigate relationships between the properties of NOM precursors and DBPs formation, and find out the optimum coagulantion conditions for efficient removal of NOM to reduce the amount of DPBs formation. The optimum conditions for the alum and ferric chloride coagulation pH for removal of NOM was 5.5 with 0.15mM coagulant dose. When adjusting pH to 5.5 with 0.15 mM ferric chloride 55% DOC removal, 81.7% THMs reduction and 89.4% HAAs reduction was achieved. when using alum 46.3% DOC removal, 70.2% THMs reduction and 74.7% HAAs reduction was achieved. The results showed that lowering pH of raw water increased the removal of NOM during coagulation process and reduced DBPs formation. Also, ferric chloride was more effectively than alum for remove NOM and reduce DBPs formation.
1. 서 론
상수원수는 그 수계의 지리적인 조건이나 주위환경에 따라 서로 다른 특성의 천연 유기물질(natural organic matter, NOM)들을 함유하고 있으며, 이런 NOM은 정수처리 공정에서 주된 처리 대상오염물질로 고려되고 있다. 또한, NOM은 각 정수공정에 대한 설계 및 운전・관리 등에도 주요변수로 작용되고 있으며, 고도정수 처리기술의 도입에도 많은 영향을 미치고 있다[1]. 이러한 NOM은 산업화, 인구의 증가 등으로 인해 수계 내 유입이 증가하고 있다. NOM은 유기물질의 복잡한 화합물 형태로 되어 있고 수생태계에 주요한 구성요소이다[2~5]. NOM은 맛, 냄새, 색도 등 수질적인 측면에서 좋지 않은 영향을 끼칠 뿐만 아니라, 급・배수관 및 물탱크 등에서 미생물의 재성장 요인이 된다. 또한 NOM은 응집제, 소독제의 주입량을 증가시키는 요소 중 하나이다.
상수원수에 존재하는 NOM은 크게 소수성(hydrophobic), 친수성(hydrophilic), 반친수성(transphilic)물질들로 이루어져 있고, 소수성 물질은 휴믹산(humic acid)와 풀빅산(fulvic acid)로 이루어져 있다. 이러한 NOM은 염소와 반응하여 700여종이 넘는 많은 소독부산물들을 생성하는데 그 중 trihalomethanes (THMs)와 haloacetic acids (HAAs)가 대체적으로 가장 높은 농도를 차지하고 있다고 알려져 있다[6]. HAAs 중 dichloroacetic acid (DCAA)와 trichloroacetic acid (TCAA)는 동물에게 발암 가능한 물질로 알려져 있다[7]. 수중의 유기물질과 염소와의 반응에 따른 염소 소독부산물 형성은 오래 전부터 haloform 반응으로 알려져 있다[8]. Haloform 반응 이외의 소독부산물 생성반응은 humic acid와 fulvic acid가 산화반응에 의해 동일한 페놀 유도체를 생성하고, 이것과 염소가 반응하여 소독부산물을 생성하는 반응이 있다[9,10]. 또한 Peters 등의 연구[11]에 따르면 humic acid의 염소처리에 의한 THMs 생성반응에 대해서 산화과정의 유무에 따라 두 가지 반응경로(전구물질-(산화)-할로겐화-가수분해-THMs 생성)를 보고한 바 있다. Croué 등과 Kavanaugh의 연구[12,13]에 따르면 일반적으로 hydrophobic 물질이 hydropilic 물질보다 THMs 및 HAAs 생성능이 높다고 보고하였으며, 반면에 Colorado 강에서는 hydropilic 물질이 hydrophobic 물질보다 THMs 및 HAAs 생성능이 높다고 보고된 바 있다[14].의 Reckhow 등의 연구[15]에 의하면 염소와 유기물질의 반응성은 humic acid, fulvic acid 순이라고 보고하였다. Humic acid에서의 THMs 생성능을 조사한 Owen 등의 연구[16]에서는 고분자 유기물질이 아닌 저분자 및 중간 분자량대의 유기물질들에서 THMs의 대부분이 생성된다고 보고한바 있으며, Chang 등의 연구[17]에서도 THMs과 HAAs를 대상으로 조사한 결과, 1 kDa 미만의 저분자 유기물질에서의 발생량이 전체의 50~74% 정도로 나타났고, 단위 DOC당 THMs과 HAAs 생성능의 경우도 1 kDa 미만의 유기물질에서 가장 높게 나타나 저분자 유기물질에서의 염소 소독부산물 생성능이 매우 높다고 보고하였다.
정수처리 공정에서 소독부산물의 생성과 제어에 대한 이슈는 기후 변화에 따른 수온 상승, 점차 강화되는 수질기준 및 신종 소독부산물의 대두와 연계되어 새로운 문제점으로 부각되고 있다[18]. 따라서 소독부산물의 전구물질인 NOM을 더 효율적으로 제거하기 위한 기술을 개발하는데 많은 관심이 집중되고 있다. NOM 제거를 위한 오존산화처리, 활성탄 흡착 등 많은 고도정수처리 기술이 있지만 본 연구에서는 이 기술들에 비해 경제적이며, 기술적으로도 대처가 용이한 응집공정에 대해 연구를 진행하였다. 또한 본 연구 대상인 낙동강 상수원수는 4대강 사업 후 수질, 특히 유기물 농도 및 성상의 변화에 많은 논란이 제기되고 있는 실정이다. 따라서 본 연구에서는 낙동강 상수원수에 함유되어있는 NOM의 효과적인 제거를 위하여 최적 응집 pH 조건에서의 DOC 제거 효율과 유기물의 성상별 소독부산물(DBPs) 생성 및 제거효과에 대해 연구하였다.
2. 연구방법
본 연구에서 사용된 낙동강 원수는 낙동강 하류 M취수장에서 취수된 원수를 사용하였으며 원수의 성상은 Table 1에 나타내었다.
2.1. 응집실험
본 연구에서 사용된 응집제는 무기 응집제중 Al계 응집제와 Fe계 응집제를 대표하는 alum (Al2(SO4)3・16H2O)과 ferric chloride (FeCl3・6H2O)를 사용하였다. 실험에 사용된 응집제는 0.25 M stock solution을 제조한 후, 10 g/L (as Al, Fe)로 희석한 dosing solution을 제조하여 하루 동안 상온에서 안정화 시킨 후 사용하였다. 응집실험은 2 L 용량의 jar를 이용하여 jar-tester (Philips & Birde, USA)를 이용하여 실험을 실시하였다. 급속혼화는 250 rpm (G=550 sec-1 at 20℃)으로 1분, 완속혼합은 40 rpm (G=36 sec-1 at 20℃)으로 20분간 진행하였고 침전시간은 30분으로 하였다. 응집시 pH는 0.5 N HCl과 0.1 N NaOH를 이용하여 조절하였다.
2.2. 유기물 분류
상수원수에 함유되어있는 유기물 특성 분류를 위해 이온교환수지인 XAD-7, XAD-4 수지를 사용하였다. XAD 이온교환수지는 humic substance의 분류를 위해서 Standard Methods로서 제안되었다[19]. DOM (Dissolved organic matter)은 유기물의 극성(polarity)과 산과 염기의 용해도에 따라 분류 할 수 있는데 본 연구에서는 XAD-7과 XAD-4 수지를 이용하여 DOM을 humic acid, fulvic acid, hydrophilic 성분으로 각각 분리하였다. DOM 분리를 위하여 시료를 0.45 μm membrane filter로 여과하고 pH 2로 산성화시킨 다음 XAD-7 수지를 통과시켜 XAD-7 수지에 흡착된 hydrophobic 물질은 0.1 N NaOH를 이용하여 탈착시켜 pH 1로 산성화시켜 안정화 시킨 후 0.45 μm membrane filter로 여과한 여액을 fulvic acid로 분류하였고, 여과지 위에 남은 잔류물은 다시 0.1 N NaOH로 용해시켜 humic acid로 분류하였다. XAD-7 수지를 통과한 여액을 XAD-4 수지에 통과시켜 나온 여액을 hydrophilic으로 분류하였다[20].
2.3. 수질 분석
Jar test 후 시료를 채취하여 탁도(HACH 2100AN), pH (Thermo ORION 4 STAR), DOC (TOC-V, Shimazu), UV254 (UV2600, Shimadzu)를 분석하였다. UV254는 시료를 GF/C 필터를 이용하여 여과한 여액을 분석하였고, DOC의 경우는 0.45 µm membrane filter를 이용하여 여과한 여액을 분석하였다. THMs 생성능은 시료를 300 mL BOD병에 채수하여 10,000 mg/L의 차아염소산 나트륨을 희석하여 잔류유리염소가 1.5±0.2 mg/L가 되도록 주입한 후 10% NaOH와 (1+10) H3PO4를 사용하여 pH를 6.8~7.2 범위로 조절한 후 20℃ 항온배양기에서 24시간 방치시킨 후 (1+10) H3PO4와 Na2SO3를 사용하여 잔류염소를 고정시킨 뒤 headspace auto sampler (HP 7964, Hewlett-packard., U.S.A)가 설치 된 GC/ECD (HP 5890 series Ⅱ, Hewlett-Packard., U.S.A)를 사용하여 분석을 실시하였다. GC/ECD에 대한 분석조건은 Table 2에 나타내었다.
3. 결과 및 고찰
3.1. 원수의 수질 특성
Fig. 1은 연구기간 중(2016년) 낙동강 취수 원수의 월별 수질 변화와 유기물의 성상별 분류를 나타낸 것이다. 탁도의 경우 3.1~26.0 NTU, DOC의 경우 2.49~3.62 mg/L로 나타났다. 본 연구에서 제시하는 결과는 수질의 변화가 크지 않은 4, 5, 6, 7, 10월의 원수를 실험 및 분석한 결과이다. Owen 등[21]은 하천수의 유기물 성상 중 hydrophobic 성분이 대략 50%라고 보고하였고, Sharp 등[22]의 연구에서는 영국 상수원수의 유기물 성상 중 hydrophobic 성분이 53~76%, hydrophilic은 21~45%라고 보고하고 있다. 본 연구결과에서도 유기물의 경우 hydrophilic 성분은 17.9~42.1%, hydrophobic 성분(fulvic acid + humic acid)은 51.5~75.1%로 유사한 결과를 나타났다. 특히 탁도, DOC와 함께 유기물의 성상도 계절별에 따라 많은 변화를 나타내었다.
3.2. NOM 제거를 위한 최적응집제 주입량
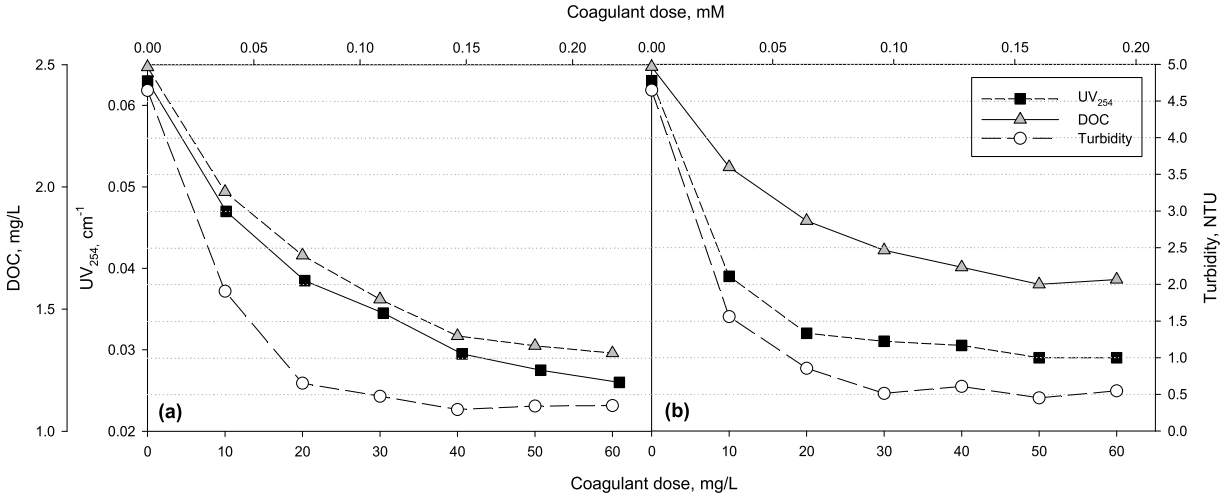
응집제별 주입량에 따른 UV254, DOC, 탁도를 Fig. 2와 같이 나타내었다. Ferric chloride의 경우 DOC의 농도를 고려하였을 때 40 mg/L에서 44.1%, alum의 경우 50 mg/L에서 35.7%로 최적 제거효율을 나타내는 것을 확인할 수 있다. Ferric chloride와 alum 응집제의 응집효율을 직접 비교하기 위하여 응집제 주입량을 금속농도로 각각 Al mM, Fe mM로 나타냈을 때 ferric chloride는 0.15 mM, alum 또한 0.15 mM로 나타났다. Christian 등[23]의 연구결과에 따르면 NOM 제거의 최적 응집제 주입량은 강화응집조건에서의 주입량과 유사하다고 보고하고 있다. 또한, ferric chloride의 경우 강화응집 조건에서 DOC의 제거율은 31~32%라고 보고되었다. Gianatasio 등[24]의 연구에서는 평균 DOC 제거율은 alum의 경우 47%, ferric chloride는 65%로 보고하였다. 본 연구에서도 ferric chloride의 경우 주입량 40 mg/L에서 44.2%, alum이 50 mg/L에서 35.7%로 나타나 ferric chloride 응집제의 NOM 응집효율이 높게 나타났다. Kang과 Han의 연구[25]에서도 alum보다 ferric chloride의 NOM 응집효율이 높다고 보고된 바 있다.
3.3. NOM 제거를 위한 최적 응집 pH
NOM 제거를 위해 최적 pH 조건을 찾기 위해 Fig. 2에서 선정된 최적 응집제 주입량 0.15 mM에서 pH를 5.0~8.0으로 조정하여 실험을 한 결과를 Fig. 3에 나타내었다. 먼저 ferric chloride의 경우 pH 5와 pH 5.5 조건에서 최고의 유기물 응집효과를 나타내었으며, alum의 경우 pH 5.5에서 최적의 유기물 제거효과를 나타내었다. 그러나 ferric chloride의 경우 pH 5 조건에서 유기물 제거효과는 뛰어나지만 탁도 제거 측면에서는 pH 5.5 조건보다 낮은 것을 나타내었다. 따라서 ferric chloride와 alum 두 응집제 모두 pH 5.5가 탁도 및 유기물 제거에 최적 응집 pH라는 것을 확인 할 수 있었다. 이처럼 동일한 응집제 주입 농도에서 pH의 변화에 따라 NOM의 제거율이 차이가 나는 것은 응집 pH에 따른 유기물의 특성변화와 형성된 알루미늄 가수분해 종들의 양전하 밀도 차로 인해 낮은 응집 pH에서 유기물 제거효율이 우수한 것으로 판단된다[26]. 일반적으로 NOM 응집 시 가장 이상적인 pH는 5.0~6.0으로 알려져 있으며[27], Christian 등[23]의 연구결과에 따르면 응집 pH는 시료와 응집제의 종류에 따라서 달라지고 최적 pH 조건은 ferric chloride의 경우 4.4~6.7, alum은 5.6~7.1이라고 보고하였다. Fig. 4는 응집제 주입량 0.15 mM에서 응집제만 주입 후 pH (ambient pH)와 조정된 pH 5.5 조건에서 각각 DOC 제거율을 나타낸 것으로, pH를 조정하지 않았을 경우 DOC 제거율은 ferric chloride의 경우 44.2%, alum의 경우 35.7%로 나타났다. 동일조건에서 pH를 5.5로 조절한 결과 ferric chloride가 55%, alum이 46.3%로 각각 10.8%, 10.6% 제거효율이 향상된 것을 확인할 수 있었다. Wang 등[28]의 연구결과에 따르면 최적 응집제 주입량은 ferric chloride는 pH 4.8, alum은 pH 5.4에서 0.25 mM로 나타났으며, ferric chloride의 경우 DOC 제거율은 70%, alum의 경우 58%로 나타났다. 본 실험에서의 결과의 제거율은 다소 다르지만 DOC 제거 경향은 유사하게 나타났다.
3.4. 유기물 성상별 생성 DBPs
수중 용존성 유기물질의 화학적 조성은 소독부산물 생성에 많은 영향을 미치는 것으로 알려져 있다[29]. Table 3은 단위 DOC당 DBPs 생성량을 나타낸 것이다. 본 실험에 사용된 상수 원수의 단위 DOC당 DBPs 생성량은 184.89 µg/mg이며, THMs는 114.35 µg/mg, HAAs는 70.54 µg/mg으로 각각 총 발생량의 61.8%, 38.2%를 차지하였다. 유기물 성상별 단위 DOC당 DBPs 발생량은 hydrophobic 132.13 µg/mg (fulvic acid: 70.98 µg/mg, humic acid: 61.15 µg/mg), hydrophilic은 52.75 µg/mg로 나타났다. THMs의 경우 hydrophobic 81.27 µg/mg (fulvic acid: 43.81 µg/mg, humic acid: 37.46 µg/mg), hydrophilic은 33.08 µg/mg, HAAs의 경우 hydrophobic 50.87 µg/mg (fulvic acid: 27.17 µg/mg, humic acid: 23.70 µg/mg), hydrophilic은 19.67 µg/mg 발생하였다. DBPs의 생성능은 hydrophobic이 hydrophilic보다 높게 나타난 것은 이전의 연구결과와 유사하며[8,28], hydrophobic 중 humic acid가 fulvic acid보다 높게 나타난다고 보고된[30] 것과는 상반된 결과를 나타났으나, 상대적으로 분자량이 큰 fulvic acid가 분자량이 작은 humic acid보다 DBPs 생성능이 높다는 결과와 같이 나타났다[16,17,30]. 또한 Krasner 등[31]이 보고한 HAAs 평균 발생량이 평균 THMs발생량의 50% 정도라는 결과와는 유사한 결과를 보였다.
3.5. DOC 제거에 따른 DBPs 생성 감소
Fig. 5는 응집제별 최적 응집 조건에서의 THMs와 HAAs의 발생 감소율을 나타낸 것이다. 최적 응집 pH인 5.5에서 THMs의 농도는 ferric chloride를 주입한 경우 97.28 µg/L에서 34.05 µg/L로 65%의 감소를 보였고, alum의 경우는 97.28 µg/L에서 37.94 µg/L로 61%의 감소를 보였다. HAAs의 농도는 ferric chloride를 주입한 경우 61.27 µg/L에서 20.21 µg/L로 67%의 감소를 보였고, alum의 경우는 61.27 µg/L에서 31.25 µg/L로 49%의 감소를 보였다. 또한 ferric chloride가 alum보다 THMs는 4%, HAAs는 18%로 보다 효과적인 것으로 나타났다. 연구결과 응집을 통한 DOC의 제거율보다 높은 DBPs 감소율을 보이는데, 이는 Table 4에서 나타낸 것과 같이 응집을 통해 제거된 DOC 중 단위 DOC당 DBPs 발생량의 약 71.5%를 차지하는 hydrophobic 물질이 응집을 통해 주로 제거되어 DBPs의 발생량이 더 감소한 것으로 판단된다. Douglas 등과 Edward 등의 연구[32,33]에서도 응집에 의한 NOM의 제거는 hydrophobic 물질의 제거효율이 hydrophilic 물질보다 높다고 보고하였다. 또한 Sharp 등의 연구[22]에서도 hydrophobic 물질이 hydrophilic 물질보다 제거효율이 높다고 보고하였으며, hydrophobic 물질 중 humic acid가 fulvic acid보다 제거효율이 높다고 보고하였다.

Comparison of DBPs reduction using 0.15 mM ferric chloride and alum at the optimum coagulation pH 5.5.
4. 결 론
소독부산물 제거를 위하여 NOM 제거를 위한 최적 응집 주입량으로 도출된 0.15 mM 농도에서 pH를 5.5로 조절한 결과를 아래와 같이 나타내었다.
1) DOC 제거율은 ferric chloride의 경우 55%, alum의 경우 46.3%로 나타났으며, 유기물 성상별 제거율은 ferric chloride의 경우 fulvic acid 58.6%, humic acid 35.6%, hydrophilic 59.5%, alum의 경우 fulvic acid 34%, humic acid 19.1%, hydrophilic 46.8% 나타났다.
2)응집공정을 통해 소독부산물의 전구물질인 NOM을 제거함으로써, THMs와 HAAs 생성은 ferric chloride의 경우 각각 65%, 67%, alum의 경우 각각 61%, 49% 감소하는 것으로 나타났다. 응집을 통해 DBPs/DOC가 높은 hydrophobic 물질이 많이 제거되어 DOC 제거 율 보다 높은 DBPs 감소율을 보였다.
본 연구의 결과를 토대로 정수처리 공정에서 응집제 종류, 주입량 및 pH조절이 고려된다면 보다 경제적이며, 기술적으로도 대처가 용이 할 것으로 기대된다.
Acknowledgements
이 논문은 2017학년도 부경대학교 연구년[Ⅱ] 교수 지원 사업에 의하여 연구되었음(C-D-2017-0373)