1. 서 론
세계적으로 원자력발전소 밀집지역인 동북아시아에 속해있는 우리나라의 수계는 인접국가에서 발생하는 재해성 원전사고, 북한의 핵 도발 및 테러 등의 위협으로부터 노출되어 있다[1]. 이러한 잠재적인 방사능 재해사고 발생 시 방사성오염물질의 유출 및 낙진으로 인해 하천 및 댐을 중심으로 한 상수원이 오염될 수 있기 때문에 비상시 방사성 오염물질을 처리할 수 있는 공정이 필요하다[2]. 137Cs은 자연환경에는 존재하지 않는 물질로 핵실험이나 원자력발전 공정을 통해 인공적으로 생성되는 방사성핵종 중 하나이다. 이러한 137Cs은 다른 방사성핵종과 비교했을 때 높은 에너지의 감마선 방출, 장반감기(약 30년), 수중에서의 높은 용해도 등의 특징을 나타낸다[3,4]. 이러한 137Cs은 수계 유입시 오염지역의 수질 및 토양 특성에 따라 용존성, 입자성으로 형태가 다르게 나타나기 때문에 137Cs의 화학적 거동을 예측하기 위해 화학적 특성이 유사한 133Cs을 활용한 연구가 활발히 진행되어 왔다[8].
137Cs의 경우 하천의 상류 및 지류지천을 통한 수계 유입 시 철저한 처리공정이 요구되지만 관련 연구 및 정보가 부족하여 신속하고 효율적인 대응이 어려운 상황이다. 또한, 정수처리시설에서 137Cs의 제거를 위해 이온교환, 막여과, 역삼투 등을 적용하고 있으나, 상수원 오염으로 인한 지속적인 유입을 처리하기 위해서는 추가적인 시설용량을 확보하고 이에 따른 높은 유지관리비용이 소요되기 때문에 137Cs 제거를 위한 현실적인 대안마련이 필요하다[5~7,13]. 반면에 흡착공정은 용존성, 입자성 137Cs 제거에 있어서 신속하고 효율적으로 활용할 수 있는 경제적인 방법이다. 이와 관련하여 수중에 존재하는 137Cs 제거를 위해 prussian blue, 이온교환수지, 천연점토광물 등을 활용한 흡착제 개발에 대한 연구가 진행되어 왔다[15~17].
Vermiculite, Illite, zeolite 등의 천연광물은 높은 이온교환능력을 가지고 있고 표면적이 크기 때문에 방사성 Cs 흡착에 효율적이라고 알려져 있다[9,10]. 특히 Illite와 zeolite는 산업적으로 유용한 물리-화학적 특성을 가지고 있고, 방사성오염물질의 높은 흡착효율을 보이는 물질로서 흡착, 촉매, 분자체 특성 등을 활용한 여러 분야에서 연구되고 있다[10,11]. Illite는 K+이온을 포함하고 있는 정장석의 풍화 또는 변질에 의해 형성되는 광물로서 방사성핵종 흡착에 효율적인 광물로 알려져 있다. 판상 구조의 형태로 이루어진 Illite 입자의 inter layer 또는 frayed edge에서 이루어지는 K+ 이온과의 이온교환을 통해 양이온성 방사성핵종인 Cs 및 Sr을 포획하여 흡착하는 특성을 가지고 있다[12]. 또한, 천연점토광물기반의 흡착제는 대량으로 보관 및 비상시 사용이 용이하고 2차적인 환경오염문제가 줄어들게 된다는 장점을 가지고 있다.
따라서 본 연구에서는 응집/침전 공정을 기반으로 개발된 수중 방사능처리장치와 천연광물인 Illite를 흡착제로 사용하여 잠재적인 방사능 재해 발생시 수계로 유입된 용존성 Cs의 효율적인 처리기술 개발에 대해 연구하고자 하였다.
2. 실험 방법 및 재료
2.1. 실험장치
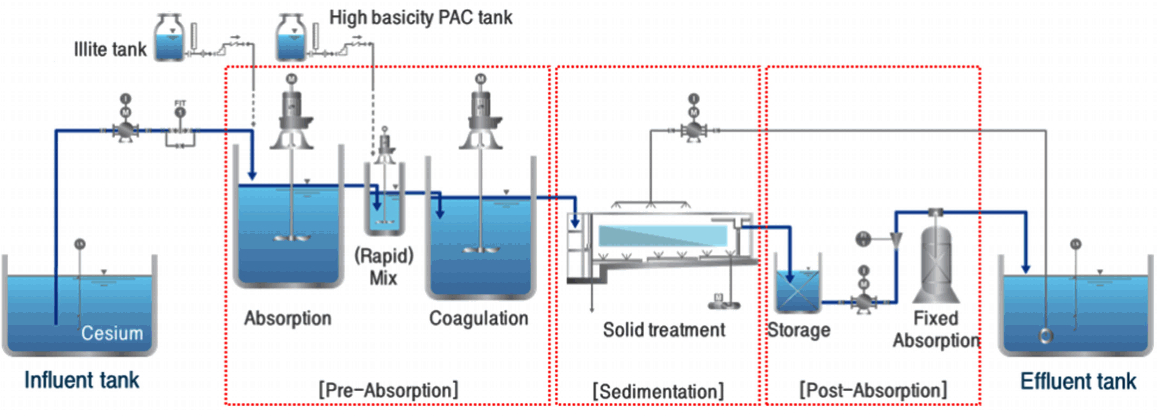
수중 방사능 처리장치 공정은 Fig. 1에 나타낸 바와 같이 전 흡착부(분말흡착조, 급속혼화조, 플럭형성조), 고형물침전부, 후 흡착부(저류조, 고정흡착탑)로 구성하였고 아크릴을 이용해 제작하였다. 1단계인 전 흡착부 공정에서 Cs 오염수(40 μg/L)는 분말흡착조(460 mm (W) × 460 mm (L) × 750 mm (H), 유효용량 160 L)로 유입되며 흡착제인 Illite는 400 mg/L의 비율로 주입되어 Cs 오염수와 혼합되었다. Cs-Illite 용액은 급속혼화조(180 mm (W) × 180 mm (L) × 300 mm (H), 유효용량 8 L) 내에서 40 mg/L의 농도를 유지하도록 일정하게 주입된 고염기도 PAC와의 반응 후 플럭형성조(500 mm (W) × 500 mm (L) × 750 mm (H), 유효용량 160 L)로 유입되어 응집교반을 통해 플력형성이 극대화 되는 과정을 거쳤다. 2단계인 고형물침전조(600 mm (W) × 1,500 mm (L) × 800 mm (H), 유효용량 720 L)는 다공성 코일형 고정상 여재의 규격에 맞추어 제작하였다. 고형물침전조에 저류된 Cs-Illite 용액은 중력에 의한 침전 및 충전된 여재에 인한 고액분리 공정을 거친 후 저류조로 유입되었다. 고형물침전조는 플럭의 침전으로 인한 단면적 감소를 고려하여 유속불균형 현상을 방지한 구조로 제작되었고 2단 월류웨어를 적용하여 침전조의 상단과 하단의 흐름이 일정한 유속으로 유지되도록 제작되었다. 3단계인 후 흡착부 공정으로 유입된 오염수는 저류조(유효용량 100 L) 내에서 유량펌프를 통해 고정흡착탑(유효용량 160 L)으로 유입되어 충전된 zeolite에 의해 2차 흡착공정을 거친 후 최종 유출되었다.
2.2. 실험재료
Cs 오염수는 하천수를 사용할 경우 입자성물질에 의한 흡착반응이 일어날 수 있으므로 수돗물을 대상으로 Cs 초기 농도를 40 μg/L로 제조하였으며, 이 때 사용된 수돗물은 pH 6.4~7.4, 수온 10℃였다. 방사성 세슘(134Cs, 137Cs)과 화학적 특성이 유사한 동위원소인 133Cs를 주입하기 위해 Cs standard 표준용액(Japan, KANTO CHEMICAL, CO., INC)을 사용하였다. 본 실험에 사용된 Illite는 국내 영동지역 광산에서 채굴된 Illite를 사용하였으며, 전 흡착부에서는 입자크기별로 LPI (Large Particle Illite, 197.4~840.9 μm)와 SPI (Small Particle Illite, 3.29~53.9 μm) 두 종류의 Illite (Korea, YONGDONG Illite CO., LTD)를 Cs 흡착제로 사용하였고 후 흡착부의 고정흡착탑에는 zeolite (Korea, PAIK KWANG INDUSTRIAL CO., LTD.)를 충전하여 2차적으로 Cs을 제거하였다. Cs이 흡착된 Illite의 회수를 위한 플럭형성을 위해 고염기도 PAC (Korea, EYOUNG CHEMICAL, CO., INC)를 응집제로 사용하였다.
2.3. 분석방법
흡착제로 사용된 Illite의 입자크기별 광물학적 형태와 표면 조성을 관찰하기 위해 전계방출형 주사전자현미경 촬영(Germany, Carl Zeiss, Feild Emission Scanning electron microscope, FE-SEM), X선 회절분석(Germany, Bruker, X-ray Diffraction, XRD)을 실시하였고, 비표면적-공극분석기(Japan, BEL, BELSORP-max)를 사용하여 질소가스의 흡착-탈착 등온선을 얻은 후 BET (Brunauer-Emmet-Teller)공식을 통해 비표면적을 측정하였다. 또한 LPI와 SPI의 평균입자크기와 분포범위 측정을 위해 입도분석(England, Malvern, mastersizer 2000)을 실시하였다.
수중 방사능 처리장치의 Cs 제거효율 측정을 위해 각 반응조별로 샘플을 채수하고 ICP-MS (USA, Agilent, ICP-MS7500)를 활용하여 Cs 농도를 분석하였다. 또한, Illite의 Cs제거효과를 비교하기 위해 전 흡착부에서 Illite 주입을 하지 않고 응집제만 주입하여 바탕실험을 하였다. 탁도는 LUTRON ELECTRONIC의 TU-2016모델을 사용하여 측정하였고 pH는 THERMO SCIENTIPIC의 STARA2155모델을 사용하여 측정하였다. 알칼리도는 SANXIN의 YD200모델을 이용해 측정하였다.
3. 결과 및 고찰
3.1. Illite의 특성분석
LPI와 SPI의 FE-SEM 분석결과를 Fig. 2에 나타내었다. (a)와 (b)는 LPI, (c)와 (d)는 SPI를 대상으로 입자구조 형태를 확인할 수 있었다. (a)와 (c)를 관찰한 결과, LPI의 경우 크기가 일정하지 않은 다양한 크기의 입자 분포를 확인할 수 있었고, 미세분말 형태인 SPI의 입자는 비교적 균일하게 분포되어 있는 것을 확인할 수 있었다. 이는 LPI의 입자 구성성분과 관련이 있다고 판단되었다. (b)와 (d)를 통해 각각 Illite의 입자구조의 형태를 확인한 결과, LPI와 SPI의 입자는 모두 일반적인 Illite 입자의 구조인 판상형태를 띄고 있는 것을 확인할 수 있었다.
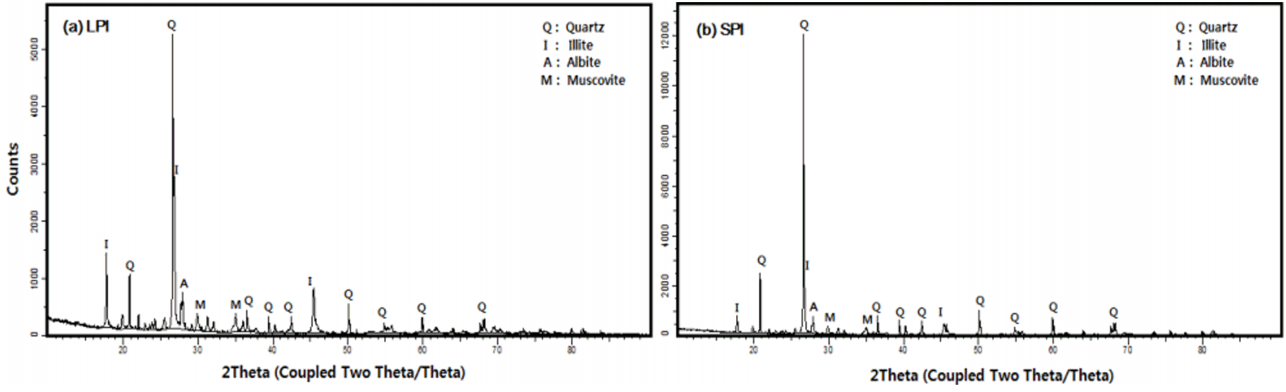
LPI와 SPI의 XRD 분석결과는 Fig. 3에서 확인할 수 있었다. LPI와 SPI의 경우 모두 같은 위치에서 Illite에 해당되는 피크가 관찰되었고 대부분 석영과 조장석 및 백운모로 구성되어 있다는 것을 확인할 수 있었다. 일반적으로 Illite 광물은 결정성이 낮기 때문에 피크의 모양이 첨도가 낮고 넓게 퍼진 형태로 나타나는데 반해, 본 실험에서 Cs의 제거를 위한 흡착제로 선정된 Illite의 경우 Illite에 해당되는 피크의 첨도가 높게 나타났다. 이는 영동지역 Illite에 sericite가 혼재되어 나타나는 영향으로 판단된다.
N2 흡탈착등온선으로부터 측정된 LPI와 SPI의 흡착 비표면적 분석결과를 Table 1에 나타내었다. BET 비표면적의 기공 부피와 평균 기공 크기는 상대압 0.993에서 N2 가스 흡착부피로부터 측정하였다. Table 1에 나타낸 바와 같이 SPI의 비표면적은 4.277 m2/g, LPI의 비표면적은 4.201 m2/g으로 나타났고 총 기공 부피는 0.018, 0.015 cm3/g, 평균 기공 크기는 16.42, 14.57 nm로 각각 측정되었다. BET분석결과 SPI에 비해 LPI의 비표면적이 낮게 나타났다. 이는 LPI의 총 기공 부피와 평균 기공 크기가 SPI에 비해 작기 때문이라고 판단되었다. 또한 LPI의 경우 일라이트 입자 이외의 모래입자 등이 혼합되어 있어 SPI에 비해 입자크기가 크기 때문에 LPI의 비표면적이 더 낮게 나타났다고 판단되었다. 입도분석을 실시한 결과를 Fig. 4에 나타내었다. SPI의 입도분포 범위의 10%에 해당하는 크기(D 0.1)는 3.287 μm, 50%에 해당하는 크기(D 0.5)는 13.24 μm, 90%에 해당하는 크기(D 0.9)는 53.87 μm로 나타났다. 반면 LPI의 입자 분포 범위의 10, 50, 90%에 해당되는 입자 크기는 197.4 μm, 556.1 μm, 840.9 μm로 각각 나타났다. 입자크기가 작은 SPI의 경우 흡착표면적이 높게 나타나고 이에 따라 상대적으로 Cs 흡착효율이 높게 측정될 것이라고 판단되었다.
3.2. 수중 방사능 처리장치의 Cs 제거효율
Fig. 5를 통해서 전 흡착부(분말흡착조, 플럭형성조), 고형물침전부, 후 흡착부(고정흡착탑) 4지점에서의 Cs 제거효율을 확인할 수 있었다. 유입된 Cs (40 μg/L) 오염수와 비교하였을 때 LPI의 주입 시 각 공정의 평균 Cs 농도는 분말흡착조 31.8, 플럭형성조 18.67, 고형물침전조 13.78, 고정흡착탑 6.87 μg/L를 나타냈다. SPI의 주입 시에는 분말흡착조 20.6, 플럭형성조 11.01, 고형물침전조 9.43, 고정흡착탑 5.77 μg/L의 평균 Cs 농도를 나타냈다. 각 공정에서의 Cs 제거효율은 Table 2에 나타낸 바와 같다. 전 흡착부 공정인 분말흡착조, 플럭형성조에서 유출수의 LPI와 SPI 주입시 각각의 Cs 제거효율은 53.3%, 72.25%였고 후 흡착부 공정인 고정흡착탑에서 2차적인 제거공정을 거친 후 최종 Cs 제거율은 82.8%, 85.7%를 나타냈다. 결과적으로 LPI와 비교하였을 때 SPI의 Cs 제거효율이 높게 나타났는데, BET분석과 입도분석 결과에서 확인된 바와 같이 SPI의 입자크기에 따른 흡착표면적이 더욱 크기 때문이라고 판단할 수 있었다.
3.3. 수중 방사능 처리장치의 탁도 제거효율
Table 3을 통해서 각각의 공정에서 탁도 변화를 확인할 수 있었다. LPI 주입시 탁도 변화를 측정하였을 때, 분말흡착조 63.06 NTU, 플럭형성조 34.54 NTU, 고형물침전조 2.71 NTU, 고정흡착탑 2.27 NTU를 나타내면서 LPI 주입시와 비교했을 때 96.4%의 탁도가 제거된 것을 확인하였다. SPI의 주입시 탁도 변화는 분말흡착조 17.24, 플럭형성조에서 0.26, 고형물침전조에서 0.23, 고정흡착탑에서 0.29 NTU를 나타내면서 SPI 주입시와 비교했을 때 약 98.3%의 탁도가 제거되는 것을 확인하였다. 탁도 제거율은 Illite에 의해 흡착된 Cs의 회수에 대해서 간접적으로 나타내는 지표로 볼 수 있다. 따라서 수중 방사능 처리장치의 운영을 통해 효율적인 흡착제 회수가 가능하다는 것을 확인할 수 있었다.
3.4. 공정 흐름에 따른 pH, 알칼리도의 변화
고염기도PAC 주입시 응집효율에 영향을 미치는 pH와 알칼리도의 변화는 Table 4를 통해서 확인할 수 있었다. 유입수와 Cs 오염수가 분말흡착조에 주입되고 LPI와 SPI가 투여되면서 평균적으로 pH 7.6~7.9의 범위를 나타냈다. 플럭형성조, 고형물침전조, 고정흡착탑의 전체적인 공정흐름에 따라 pH 변화 범위는 SPI의 경우 약 6.5, LPI의 경우 약 6.8로 낮아졌고 고형물침전조 이후의 공정에서는 유사한 범위로 유지되는 경향을 보였다. LPI 주입시 알칼리도는 분말흡착조 49.75, 플럭형성조 32.27, 고형물침전조 30.63, 고정흡착탑 29.56 mg/L as CaCO3를 나타냈다. SPI의 주입시 알칼리도 측정 농도는 분말흡착조 47.72, 플럭형성조 18.01, 고형물침전조 19.81, 고정흡착탑 18.90 mg/L as CaCO3로 나타났다. 일반 응집제의 주입시 pH의 경우 5 이하로 낮아지고 알칼리도 역시 5 mg/L CaCO3 이하로 낮아지는 경향을 보인다. 이렇게 pH와 알칼리도가 낮게 형성되면 응집제의 수화반응을 급격히 저하시키게 되면서 전체적으로 응집효율은 떨어지게 된다고 알려져 있다. 하지만 고염기도 응집제의 주입시 pH는 6.5 정도로 유지되고 알칼리도의 소모 역시 크지 않다고 알려져 있다[18]. 본 실험에서는 응집제로 사용된 고염기도PAC의 주입으로 인해 pH와 알칼리도의 급격한 감소를 제어할 수 있었고 이를 바탕으로 높은 탁도 제거율이 나타났다고 판단하였다.
4. 결 론
본 연구에서는 방사능 재해시 수계로 유입된 Cs의 제거를 목적으로 개발된 수중 방사능 처리장치의 운영을 통해 용존성 Cs 제거효율을 측정하였다. 수중 방사능 처리장치의 전체적인 공정은 전 흡착조(흡착조, 플럭형성조), 고형물침전조, 후 흡착조(고정흡착탑) 공정으로 나누어 볼 수 있었다. 방사성 오염물질인 134Cs, 137Cs과 화학적 특성이 유사한 동위원소인 133Cs를 사용하여 실험을 진행하였고 천연광물인 Illite를 흡착제로 사용하였다. 또한 고염기도PAC를 응집제로 사용하여 탁도 제거를 통해서 흡착제로 사용된 Illite의 회수를 간접적으로 확인하고자 하였다. 흡착제로 사용된 Illite 2 종류의 특성분석을 실시하였고 수중 방사능 처리장치의 각 반응조별로 샘플을 채수하여 Cs의 제거효율을 검토하였다. 이에 대한 분석 및 실험결과는 다음과 같이 판단할 수 있었다.
1) FE-SEM 분석결과, LPI 및 SPI의 입자크기의 분포는 각각 다르게 나타났지만 입자의 구조는 동일하게 판상형태를 나타내는 것을 확인할 수 있었다. XRD 분석결과, 두 종류의 Illite 모두 Illite에 해당하는 피크가 관찰되었고 동일 물질로 구성되어 있다는 것을 확인할 수 있었다. 본 실험에서 흡착제로 선정된 충북 영동지방에서 생산되는 Illite는 일반적인 Illite와는 다르게 sericite가 혼재되어있어 Illite에 해당되는 피크의 첨도가 높게 나타난 것이라고 판단되었다. BET 분석결과 LPI, SPI의 흡착 비표면적은 각각 4.201 m2/g, 4.277 m2/g으로 나타났고 총 기공 부피와 평균 기공 크기를 확인했을 때 SPI의 측정값이 상대적으로 높게 나타났다. 입도분석결과를 살펴보았을 때 LPI, SPI의 입자크기분포는 각각 3.29~53.58 μm, 197.4~840.9 μm를 나타냈다.
2) 수중 방사능 측정장치의 Cs 제거효율을 측정한 결과 전 흡착부 공정(분말흡착조, 플럭형성조)에서 고형물 침전조를 거치면서 Illite 주입시와 비교했을 때, SPI의 경우 76.4%, LPI의 경우 약 65.5%의 제거율을 나타냈다. 후 흡착부 공정인 고정흡착탑을 거치면서 유입 Cs (40 μg/L) 농도와 비교하였을 때 85.6%, 82.8%의 제거율을 각각 나타냈다. 결과적으로 SPI의 Cs 제거효율이 더 높게 나타났는데, 이는 BET 비표면적 분석과 입도분석을 통해 측정된 결과와 관련있다고 판단하였다.
3) 수중 방사능 측정장치의 탁도 제거효율을 측정한 결과 LPI의 주입시 분말흡착조에서 63.06 NTU를 나타냈고 최종 유출수의 경우 2.27 NTU를 나타내면서 96.4%의 탁도제거율을 나타냈다. SPI의 주입시 분말흡착조에서 17.24 NTU의 탁도가 최종 유출수에서 0.29 NTU를 나타내면서 98.3%의 탁도 제거율을 나타냈다. 이를 통해 수중 방사능 처리장치의 운영을 통해 효율적인 흡착제의 회수가 가능할 것이라고 판단되었다.
4) 수중 방사능 측정장치 운영에 있어서 응집제로 사용한 고염기도 PAC의 주입을 통해 플럭형성조에서 고정흡착탑에 이르기까지 각 공정에서의 pH 및 알칼리도의 급격한 감소를 제어할 수 있었다. 이를 통해 플럭형성이 원활하게 이루어졌고 높은 탁도제거율을 나타냈다고 판단하였다. 하천수의 특성에 따른 경쟁이온 및 유기물, 입자성 물질의 존재시 Cs의 제거효율이 상이하게 나타날 수 있다. 따라서 향후 하천 현장에서의 Cs 제거효율을 평가하기 위해 다양한 환경 및 수질의 특성을 고려한 추가적인 실험이 필요할 것이라고 판단된다.