The Korean text of this paper can be translated into multiple languages on the website of http://jksee.or.kr through Google Translator.
생물활성탄 공정에서 Geosmin과 MIB의 제거 특성: 생물분해와 흡착
Abstract
We evaluated geosmin and MIB biodegradation and adsorption mechanism of biological activated carbon (BAC) and anthracite biofilter. In steady state of BAC process, the geosmin and MIB were completely removed at the 30 min empty bed contact time (EBCT) even though low water temperature (9℃) in which the activity of attached bacteria decreased. When the water temperature was 26℃, the microbial biomass and activity were higher at the upper layer of the biofilm than at 9℃, and the microbial biomass and activity decreased as the depth was deeper. This is because when the water temperature is high, the biodegradable organic matter (BOM) removal rate in the upper layer is high and the BOM amount that can’t be supplied to the lower layer. The Removal rate of geosmin and MIB by BAC process did not show a significant difference compare to activity-inhibited BAC by treated with azide and the biofilter also removed the geosmin and MIB by biological action. It means geosmin and MIB could be removed by competitive relationship between adsorption and biodegradation.
Key words: Geosmin, MIB, Biological Activated Carbon, Adsorption, Biodegradation
요약
본 연구에서는 생물활성탄 공정에서 geosmin과 MIB의 제거시 생물분해와 흡착기작의 역할을 BAC와 biofilter를 이용하여 평가하였다. 정상상태에 도달한 BAC 공정에서 부착 박테리아들의 활성이 저하된 저수온기(9℃)에도 EBCT 30분의 조건에서는 geosmin과 MIB가 완전 제거되었다. 유입수의 수온이 26℃일 때가 9℃일 때보다 상층부분에서 부착 박테리아의 생체량과 활성도가 높았고, 여층의 하부로 갈수록 부착 박테리아의 생체량과 활성도의 감소율이 높게 나타났다. 이는 수온이 높을 때 상층부분에서 BOM 제거율이 높아 하층에 공급할 수 있는 BOM 양이 감소하기 때문이다. 부착 박테리아의 활성이 억제된 BAC 공정의 geosmin과 MIB의 제거율은 활성화된 BAC 공정에서의 제거율과 비교하여 큰 차이를 나타내지 않아 BAC 공정에서 geosmin과 MIB의 제거에 흡착기작의 기여도가 높게 나타났다. BAC 공정에서 geosmin과 MIB의 제거시 부착 박테리아에 의한 생물분해 기작과 활성탄 표면이 가지는 흡착 기작이 경쟁적으로 작용하였다.
주제어: Geosmin, MIB, 생물활성탄, 흡착, 생물분해
1. 서 론
상수원수 중에는 다양한 기원으로 맛과 냄새를 유발하는 이취 물질들이 잔존한다. 특히, 조류(algae)와 방선균에서 기인하는 trans-1-10-dimethyl-trans-9-decalol (geosmin)과 2-methylisoborneol (MIB)의 경우 역치농도(threshold concentration)가 6~10 ng/L p[ 1, 2] 정도로 매우 낮고, 재래식 정수처리공정에서의 낮은 제거능[ 3, 4]으로 인해 수돗물에 대한 민원 및 불신을 유발하는 대표적인 이취미 물질들이다[ 5]. 따라서 미국과 유럽 등의 여러 선진국들에서는 정수처리 공정에서 이취물질들의 제거를 위해 많은 투자와 관심을 기울이고 있다[ 5, 6]. 최근 몇 년 사이에 국내 대부분의 상수원에서 조류가 대량으로 발생하는 현상이 빈번히 보고되고 있으며, 조류가 영향을 미치는 상수원에 위치한 정수장에서는 하절기에 조류 기인 geosmin과 MIB로 인해 정수장 운영에 많은 어려움을 야기하고 있다. 정수처리 공정에서의 geosmin이나 MIB의 제어를 위해 산화[ 7~ 9], 흡착[ 10~ 12] 및 생물학적 처리공정[ 13, 14]에 대한 많은 연구가 수행되었다. 특히, 생물활성탄(biological activated carbon, BAC) 공정과 생물여과 공정과 같은 생물학적 처리공정에서의 geosmin과 MIB의 제거연구를 수행한 Elhadi 등[ 15]과 Meyer 등[ 16]의 연구결과에서 다양한 수온, 유입농도, 여재 종류 및 BOM 농도 조건에서 geosmin과 MIB가 효과적으로 생물분해되는 것으로 보고하고 있다. 지방족 고리를 가진 알콜류의 일종인 geosmin은 여러 단계의 탈수소 효소 반응(dehydrogenase reaction) 및 단일산소첨가 효소반응(monooxygenase reaction)을 거치며 생물분해되며, 두 고리(bicyclic) 화합물인 MIB의 경우는 생물분해에 의해 단일산소화 효소반응 단계들을 거치며 개환(ring cleavage) 및 무기화된다[ 17]. 국내의 대규모 정수장에서는 geosmin과 MIB와 같은 미량 오염물질들의 제거를 위해 오존/생물활성탄 공정을 채택하여 운전하고 있다. 생물활성탄(BAC) 공정은 입상활성탄 공정을 장기간 운전할 경우 입상활성탄의 표면과 세공에 종속 영양성 박테리아들이 자연적으로 부착, 군집을 형성하여 생물학적 분해능을 제공한다. 따라서 생물활성탄은 수중의 유기성 오염물질 제거시 입상활성탄이 가지는 흡착 기작과 부착박테리아들에 의한 생물분해 기작이 동시에 유발되어 유기성 미량오염물질들에 대해 높은 제거능을 나타낸다[ 18, 19]. 본 연구에서는 유기성 미량오염물질들의 제거를 위해 국내의 대규모 정수장들에서 운전되고 있는 생물활성탄 공정에서 geosmin과 MIB의 제거시 생물분해와 흡착의 기여율을 평가하여 하절기 생물활성탄 공정이 채택된 정수장에 geosmin과 MIB의 유입시 이들의 제거를 위한 BAC 공정 운영의 기초자료로 활용하고자 하였다.
2. 실험재료 및 방법
2.1. 실험재료
2.1.1. 유입수 성상
유입수는 고도정수처리용 pilot-plant의 후오존 처리수에 순도 99% 이상의 geosmin과 MIB (sigma-aldrich)를 투입하여 BAC와 biofilter로 유입되는 geosmin과 MIB의 농도를 각각 30 ng/L가 되도록 하였다. 실제 정수장의 BAC 공정과 동일한 조건으로 하기 위해 후오존 처리수를 유입수로 사용하였으며, 실험기간 중 후오존 처리수의 성상을 Table 1에 나타내었다. 유입수의 수온은 수온조절 장치(Buchi, Recirculating chiller B-740, Swiss)를 이용하여 9℃와 26℃로 조절하여 실험하였다. 유입수의 BOM 농도를 증가시키기 위해 sigma-aldrich사에서 제조한 순도 99% 이상의 formaldehyde, glyoxal, formate 및 acetate를 Urfer가 제시한 방법[ 20]으로 조제한 후 유입수에 첨가하였다. BOM 시료수는 formaldehyde 100 µg/L, glyoxal 30 µg/L, formate 400 µg/L 및 acetate를 300 µg/L의 농도로 투입하여 후오존 처리수의 BDOC 농도를 280 µg/L 정도 증가시켰다[ 20]. 수중의 유기탄소 성분이 박테리아 생장의 제한인자가 되도록 sigma-aldrich사에서 제조한 순도 99.5% 이상의 NaNO 3와 K 2HPO 4를 Urfer가 제시한 방법[ 20]으로 조제한 후 유입수에 첨가하였다. 박테리아 세포의 경험적인 분자식은 C 55H 77O 22N 11P 2이며[ 21], 박테리아가 세포 구성물질로 섭취하는 C:N:P의 비율은 21 : 5 : 1 (w/w/w)로 표현된다. 본 연구에서도 모든 실험조건에서 C:N:P의 비율을 15 : 5 : 1 (w/w/w)로 조절하여 유기탄소가 박테리아 생장의 제한인자가 되도록 하였다[ 20].
2.1.2. BAC와 Biofilter 여재
BAC는 석탄계(coal) 재질 활성탄(F400, Calgon)을 사용하였으며, biofilter 여재로는 안트라사이트(한국 안트라사이트)를 사용하였다. BAC 및 안트라사이트는 낙동강 원수를 정수처리하는 300톤/일 처리규모의 pilot-plant의 후오존/BAC 및 후오존/biofilter 공정에서 2년간 사용한 것이다. 활성탄과 안트라사이트 여과지에서 실험에 사용할 BAC와 biofilter 여재를 채집하여 각각의 bench-scale의 아크릴 컬럼에 충진한 후 geosmin과 MIB에 대한 순응을 위해 유입수로 사용한 후오존 처리수에 geosmin과 MIB를 각각 30 ng/L~35 ng/L 농도범위로 투입하여 수온 20±3℃의 조건에서 4주간 운전하면서 순응기간을 거쳤다.
2.2. 실험방법
2.2.1. BAC와 biofilter 공정 운전
본 실험에 사용된 bench-scale BAC와 biofilter 컬럼은 아크릴 재질의 내경 7 cm, 높이 200 cm 규모이고, 채집된 활성탄과 안트라사이트 여재를 각각 층고 100 cm로 충진하였다. 잔류오존이 제거된 후오존 처리수는 집수조로 이송된 후 수온조절장치을 거친 후 펌프로 BAC와 biofilter 컬럼의 상부로 이송되며, 이송 라인 중간에 geosmin, MIB, BOM 및 부착 박테리아의 활성저해제로 사용한 NaN 3 용해액 유입펌프가 연결되어 있어 주입된 이들 용액들이 상부에 설치된 혼화조에서 완전히 혼화된 후 각각의 BAC와 biofilter 여과지로 유입되도록 설계하였으며, 접촉조의 상부에는 유입수의 수온을 측정하는 온도계가 설치되어 있다. 접촉조의 운전은 하향류식으로 운전하였으며, 공탑체류시간(empty bed contact time, EBCT)은 3분(층고 10 cm)~30분(층고 100 cm)이 되도록 운전하였고, 역세척은 염소처리 공정이 배제된 pilot-plant의 최종 처리수를 사용하여 주 1회 정도로 수세와 공세를 병행하여 실시하였다. 활성탄 BAC와 biofilter 컬럼의 상세한 설계인자를 Fig. 1에 나타내었다.
2.2.2. 분석
Geosmin과 MIB의 분석은 polydimethylsiloxane (PDMS)이 코팅되어 있는 교반막대(Twister TM, Gerstel, Germany)에 geosmin과 MIB를 흡착시켜 수중에서 분리하는 교반막대 흡착추출법(stir bar sorptive extraction: SBSE)을 전처리 법으로 사용하여 GC-MSD로 분석하였다[ 22]. Geosmin과 MIB 전처리는 시료수 10 mL를 20 mL vial에 취하여 염석제로 NaCl 3 g을 투입한 후 길이 10 mm, 두께 3.2 mm인 교반막대를 투입하여 1200 rpm으로 90분 동안 회전시키면서 시료수에 함유된 geosmin과 MIB를 흡착·추출하였다. Table 2에는 GC-MSD의 분석조건을 나타내었다. BAC와 biofilter 부착 박테리아의 생체량 측정에는 ATP법을 이용하였다. 여재 습중량 200 mg을 채집하여 Velten 등이 제시한 방법[ 23]을 이용하여 전처리한 후 분석하였으며, ATP standard (Promega, USA)를 이용하여 ATP 농도 검량선을 작성하였고, luminometer (Victor3, PerkinElmer, USA)를 이용하여 ATP 농도를 측정하였다. 부착 박테리아의 활성도는 3H-thymidine이 DNA에 흡수되는 정도로 구하여 평가하였다[ 24]. 먼저 여재 습중량 1 g을 초음파 처리하여 박테리아를 탈리시킨 시료 2 mL에 200 nM [methyl- 3 H] thymidine 용액(specific activity: 40~50 Ci/mmol) 1 mL와 200 nM cold thymidine 용액 1 mL를 첨가한 후 교반 배양기에서 in situ 조건으로 4시간 배양하였다. ATP 용액(25 g/L) 100 µL와 1 N NaOH 2 mL를 첨가하여 100℃에서 1시간 동안 가열하여 DNA를 추출·냉각·원심분리하였다. 상등액 1 mL에 ice-cold 10% trichloroacetic acid 5 mL를 첨가하여 15분 정도 냉각시킨 후 0.2 µm 멤브레인 필터로 여과하였다. 이 여지를 vial에 넣고 건조시킨 후 ethyl acetate 1 mL와 10 mL의 scintillation cocktail (Aquasol-2, Packard)을 주입하여 liquid scintillation analyzer (PerkinElmer, Quantulus 1220, USA)로 방사선량을 측정하였다. 얻어진 DPM (disintergrate per minute) 값으로부터 Parsons 등[ 25]이 제시한 식을 이용하여 세균에 결합된 thymidine의 양을 계산하여[ 26], 계산된 값을 여재 g당 생체량(ATP 농도)으로 환산하여 나타내었다.
3. 결과 및 고찰
3.1. 수온 변화에 따른 geosmin과 MIB 제거 특성
유입수의 수온변화(9℃와 26℃)에 따른 BAC와 biofilter에서의 geosmin과 MIB의 제거 특성을 Fig. 2에 나타내었다. BAC와 biofilter 모두 EBCT 30분의 조건에서 채수하여 분석하였다. BAC의 경우 유입수의 수온에 관계없이 geosmin과 MIB가 모두 제거되었으며, biofilter에서는 수온이 9℃일 때 평균 geosmin과 MIB의 제거율이 88%와 77%로 나타났으나 수온이 26℃로 높을 경우에는 geosmin과 MIB가 모두 제거되었다. 이와 같이 BAC 공정에서는 수온변화에 관계없이 일정한 제거율을 나타낸 반면 안트라사이트 여재로 사용한 biofilter에서는 수온이 저하됨에 따라 제거율의 감소가 유발되었다. 일반적으로 biofilter 공정에서의 유기 물질 제거능의 경우, 수온의 저하가 부착 박테리아의 생체량과 활성도의 저하에 직접적인 영향을 미치기 때문에 수온 변화에 매우 의존적이다[ 27]. 그러나 BAC 공정에서는 수온이 9℃로 저하되어도 geosmin과 MIB의 제거율에는 거의 변화가 나타나지 않아 BAC 공정에서는 geosmin과 MIB의 제거시 생물학적인 제거기작 뿐만 아니라 수온의 영향을 받지 않는 물리·화학적인 제거기작도 관여하는 것으로 평가되었다.
3.2. 수온 변화에 따른 생물막 특성 평가
BAC에서의 유입수의 수온 변화에 따른 여층별 부착 박테리아의 생체량과 활성도를 평가한 것을 Fig. 3(a)에 나타내었다. 부착 박테리아들의 생체량은 수온에 관계없이 여층의 상층(-5 cm)에서 하층(-90 cm)으로 갈수록 점진적으로 감소하였고, 수온 저하에 따라 하층에 비해 상층의 생체량 감소율이 크게 나타났다. 또한, 수온 변화에 따른 여층별 부착 박테리아 활성도의 경우도 수온이 낮아질수록 하층에 비해 상층에서의 활성도 감소율이 크게 나타났고, 수온이 높을수록 상층과 하층의 활성도 차이가 크게 나타났다. 수온 변화에 따른 여층 깊이별 생체량과 활성도의 변화를 보면 상층에 비해 하층에서 큰 차이를 유발하지 않은 이유는 수온 26℃에서는 높은 수온에 따른 BAC 여층 상층부의 부착 박테리아의 생체량과 활성도가 높아서 생물분해 가능한 유기물질(BOM)의 소비율이 높기 때문에 하층부로 유출되는 BOM 양이 감소하여 하층부에 서식하는 박테리아들의 유기 탄소원의 농도 감소로 인해 생체량과 활성도에 제한을 받았다( Fig. 3(b)). 그러나 수온이 9℃로 낮은 경우는 유입수의 수온 저하로 인해 상층부에 부착된 박테리아들의 생체량과 활성도 저하로 BOM의 소비율이 감소하여 하층부까지 BOM이 전달되기 때문에 컬러의 하층부에서는 수온 26℃일 때와 유사한 생체량과 활성도를 유지하는 것으로 판단된다( Fig. 3(b)).
Table 3에는 수온 변화에 따른 BAC와 biofilter 부착 박테리아들의 여층별 생체량과 활성도를 비교한 것을 나타내었다. BAC와 biofilter의 생체량의 경우, 수온 9℃에서 여층의 상층부와 하층부에서 각각 1.82와 1.10 µg·ATP/g·GAC 및 0.81과 0.50 µg·ATP/g·anthracite로 나타났고, 수온 26℃ ATP/g·anthracite로 나타나 활성탄과 안트라사이트의 단위 무게(g)당 생체량에는 큰 차이를 나타내었다.
활성탄은 수많은 세공으로 이루어진 다공질체여서 안트라사이트의 겉보기 비중인 0.9 g/mL에 비하여 석탄계 재질 활성탄의 경우 0.42 g/mL이다. 따라서 활성탄과 안트라사이트 부착 박테리아의 단위 무게당 부착 박테리아의 생체량을 단위 부피(mL)당 생체량으로 환산한 것을 Table 3의 괄호로 나타내었으며, 환산된 값을 보면 활성탄과 안트라사이트에서의 단위 부피당 생체량이 여층의 상층과 하층에서 거의 유사하게 나타나고 있다. 활성탄과 안트라사이트에 부착된 박테리아들의 활성도는 여재 단위 무게당 부착된 박테리아들을 탈리시켜 방사능 동위원소인 3H-thymidine이 박테리아들의 DNA에 흡수되는 정도로 구하여 생체량(ATP) 무게당으로 환산하여 나타내었다. BAC와 안트라사이트 부착 박테리아들의 활성도는 상층과 하층 모두에서 큰 차이를 나타내지 않았다.
3.3. 부착 박테리아 활성 억제에 따른 geosmin과 MIB 제거 특성
활성억제제인 NaN 3를 이용하여 BAC와 biofilter 부착 박테리아들의 활성 억제 전·후의 geosmin과 MIB 제거 특성을 평가한 것을 Fig. 4(a)~ (d)에 나타내었다. BAC 공정에서의 NaN 3 투입 전·후의 geosmin과 MIB 제거 특성을 평가한 Fig. 4(a)와 (b)를 보면 NaN 3를 투입하여 부착 박테리아들의 활성을 억제시킨 경우에도 NaN 3 투입 전과 비교하여 geosmin의 제거율에는 큰 변화는 없었으나 MIB의 제거율은 다소 감소하였다. 그러나 Fig. 4(c)와 (d)에 나타낸 biofilter에서의 NaN 3 투입 전·후의 geosmin과 MIB 제거 특성을 평가한 결과에서는 NaN 3 투입으로 인해 부착 박테리아들의 활성이 억제되어 geosmin과 MIB의 제거율에는 많은 차이를 나타내었다. 따라서 biofilter 공정에서의 geosmin과 MIB의 제거는 전적으로 생물분해 기작에 의한 것을 알 수 있으며, 여재(안트라사이트) 또는 생물막에 흡착된 정도는 5~6% 정도로 나타나 주목할 만한 정도로 평가되지는 않았다. 앞에서 언급하였듯이 BAC 공정에서 NaN 3 투입으로 MIB의 제거율은 다소 감소된 반면 geosmin의 제거율에는 거의 변화가 없었던 것은 geosmin의 제거에 있어서 흡착이 매우 큰 영향을 미치는 것을 의미한다. Geosmin과 MIB의 Log Kow값은 각각 3.7과 3.13으로 geosmin이 MIB에 비해 흡착에 유리한 물리·화학적 특성을 가진다[ 28]. 또한, 이전의 여러 연구 결과들에서도 MIB에 비해 geosmin이 활성탄 흡착제거가 용이하다는 결과를 보고하고 있다[ 10, 29]. 부착 박테리아들의 활성이 억제된 BAC, 즉 흡착 기작만이 작용하는 BAC 공정과 부착 박테리아들이 활성화되어 있는 biofilter, 즉 생물분해가 주 제거기작인 biofilter 공정에서의 geosmin과 MIB의 제거능을 비교해보면 여층의 변화에 따른 제거율의 변화 특성이 매우 유사한 것을 볼 수 있다. 이것은 BAC 공정에서 geosmin과 MIB 제거시 생물분해와 흡착 기작이 매우 유사한 비율로 기여한다는 것을 의미한다. Fig. 5에 나타낸 Son 등의 연구[ 30]에서 보고한 BAC 공정에서 채취한 활성탄을 주사전자 현미경으로 관찰한 사진을 보면 활성탄에 부착된 박테리아들이 활성탄 표면에 듬성듬성 존재하는 것을 볼 수 있다. 따라서 물과 접촉할 수 있는 활성탄 표면은 충분히 존재하기 때문에 Fig. 4에서와 같이 geosmin과 MIB에 대한 흡착능을 가진다. 또한, 앞의 Table 3에서 볼 수 있듯이 BAC와 biofilter 공정의 여재에 단위 부피당 부착된 생체량과 활성도의 결과는 매우 유사하게 나타나 정상상태(NaN 3 투입 전)의 biofilter가 BAC 공정과 유사한 생물분해능을 가진다고 평가할 수 있다. 따라서 BAC 공정에서 geosmin과 MIB의 제거시 부착 박테리아들에 의한 생물분해 기작과 활성탄 표면이 가지는 흡착 기작은 경쟁적으로 작용하는 것을 알 수 있다. Drikas 등[ 31]의 연구결과에서는 geosmin의 주요 제거 메카니즘은 흡착인 반면, MIB의 경우는 생물분해인 것으로 보고하고 있다.
4. 결 론
BAC 공정에서 geosmin과 MIB의 제거시 생물분해와 흡착기작의 역할을 BAC와 biofilter를 이용하여 평가해 본 결과, 다음과 같은 결론을 얻을 수 있었다.
1) 정상상태에 도달한 BAC 공정에서 부착 박테리아들의 활성이 저하된 저수온기(9℃)에도 EBCT 30분의 조건에서는 geosmin과 MIB가 완전 제거되었다.
2) BAC 공정에서 고수온기(26℃)에 비해 저수온기(9℃)에 여층 상층부의 부착 박테리아의 생체량 감소율과 활성도 저하율이 여층의 하층부에 비해 상층에서 높게 나타났고, 저수온기에는 고수온기에 비해 하층으로 유입되는 BOM의 농도가 상승하여 생체량과 활성도의 저감율이 감소하였다.
3) 부착 박테리아들의 활성이 억제된 BAC 공정의 geosmin과 MIB의 제거율은 활성화된 BAC 공정에서의 제거율과 비교하여 큰 차이를 나타내지 않아 BAC 공정에서 geosmin과 MIB의 제거에 흡착기작의 기여도가 높게 나타났다.
4) BAC 공정에서 geosmin과 MIB의 제거시 부착 박테리아에 의한 생물분해 기작과 활성탄 표면이 가지는 흡착 기작은 경쟁적으로 작용하였다.
Fig. 1.
Schematic diagram of bench-scale BAC and biofilter. 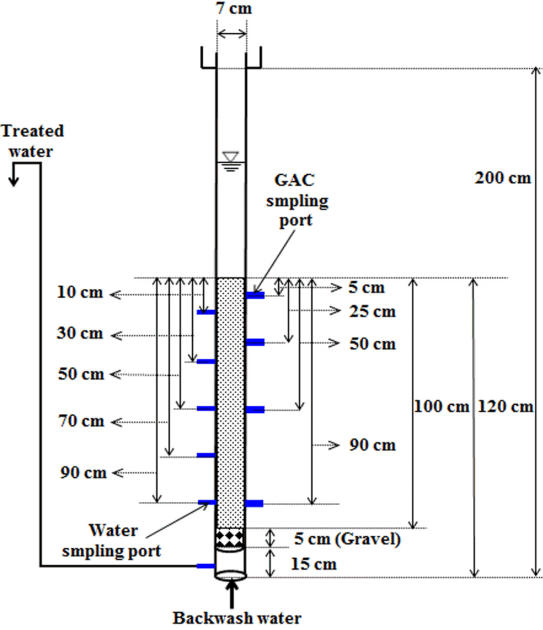
Fig. 2.
Average removal of geosmin and MIB in the BAC and biofilter during summer and winter season, measured at 100 cm bed depth corresponding to 30 min EBCT. 
Fig. 3.
Biofilm characteristics and BOM removal of BAC process as a function of bed depth at water temp. 26℃ and 9℃. 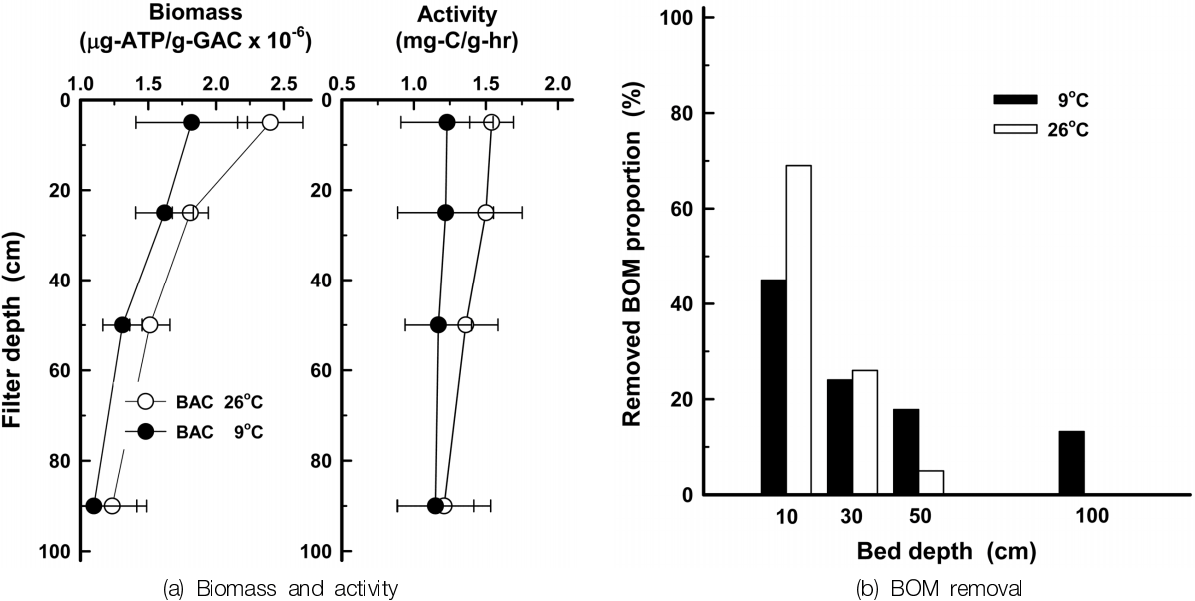
Fig. 4.
Residual ratios of geosmin and MIB during normal condition and azide dosing condition of BAC and biofilter. (water temp.: 26℃). 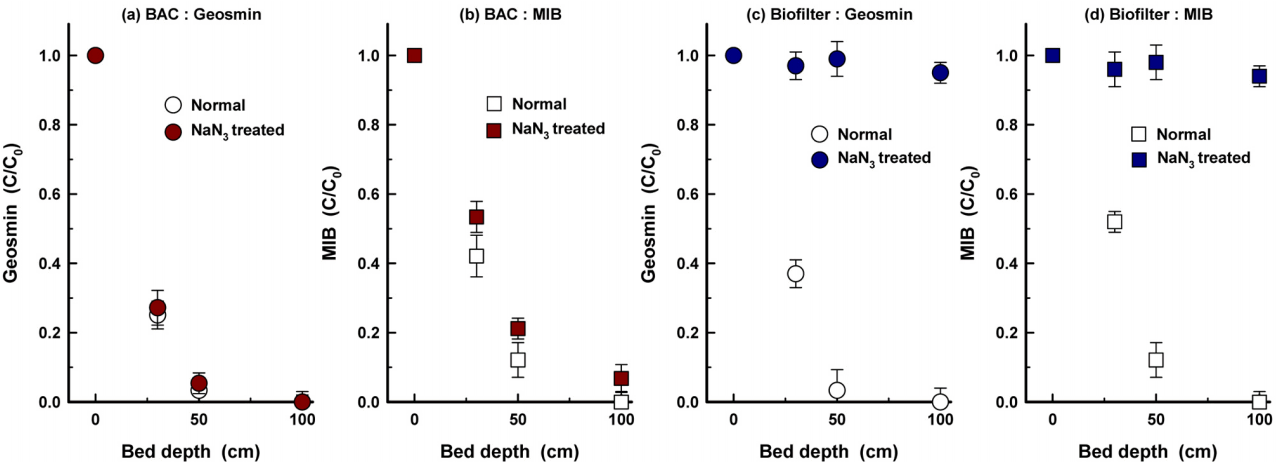
Fig. 5.
Scanning electron microscopy of BAC bed[ 30]. 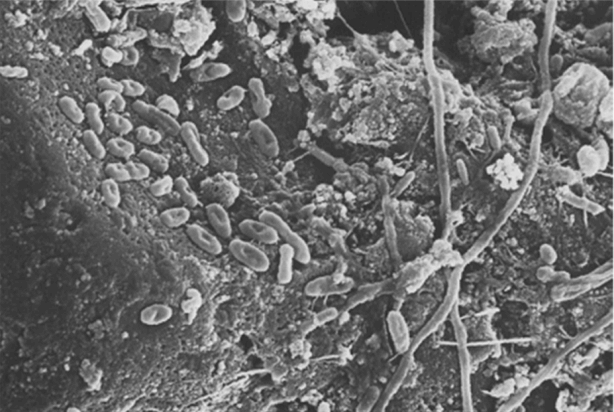
Table 1.
Characteristics of post ozonated water
|
Parameters |
pH
|
Turbidity
|
DOC
|
BDOC
|
|
(-) |
(NTU) |
(mg/L) |
(mg/L) |
|
Value |
7.1~7.8 |
0.04~0.08 |
1.25~1.57 |
0.26~0.41 |
Table 2.
Analytical conditions of the GC/MSD
|
• GC (6890N, Agilent, USA) |
|
- Column: HP-5MS, 30 m (L) ×0.25 mm (ID) ×0 .25 μm (film thickness) |
|
- Oven Temp.: Initial Temp. 50℃, Hold 1.6 min, |
|
- 1st rate 20℃ to 100℃, 2nd rate 10℃ to 140℃, 3rd rate 5℃ to 160℃ |
|
• MSD (5973N, Agilent, USA) |
|
- SIM mode |
|
- Selected ion: geosmin (111, 112, 125), 2-MIB (95, 108) |
Table 3.
Biomass and activity of BAC bed as a function of bed depth during summer and winter season
|
Water temp. |
BAC
|
Biofilter
|
Biomass (μg∙ATP/g∙GAC)
|
Activity (mg∙C/g∙hr)
|
Biomass (μg∙ATP/g∙anthracite)
|
Activity (mg∙C/g∙hr)
|
|
Top (5 cm) |
Bottom (90 cm) |
Top (5 cm) |
Bottom (90 cm) |
Top (5 cm) |
Bottom (90 cm) |
Top (5 cm) |
Bottom (90 cm) |
|
9℃ |
1.82 (0.77) |
1.10 (0.46) |
1.23 |
1.15 |
0.81 (0.74) |
0.50 (0.45) |
1.12 |
1.14 |
|
26℃ |
2.40 (1.01) |
1.23 (0.52) |
1.54 |
1.21 |
1.05 (0.95) |
0.52 (0.47) |
1.44 |
1.17 |
References
1. A. K.. Meng, I. H.. Suffet, A procedure for correlation of chemical and sensory data in drinking water samples by principal component factor analysis, Environ. Sci. Technol., 31, 337-345(1997).  2. D. M. C.. Rashash, A. M.. Dietrich, R. C.. Hoehn, FPA of selected odorous compounds, J. Am. Water Works Assoc., 89, 131-141(1997).
3. S.. Lalezary, M.. Pirbazari, M. J.. McGuire, Evaluating activated carbons for removing low concentrations of taste-producing and odor-producing organics, J. Am. Water Works Assoc., 78(11), 76-82(1986).
4. A. U.. Wnorowski, Tastes and odors in the aquatic environment: a review, Water SA., 18(3), 203-214(1992).
5. I. H.. Suffet, A.. Corado, D.. Chou, M. J.. McGuire, S.. Butterworth, AWWA taste and odor survey, J. Am. Water Works Assoc., 88, 168-180(1996).
6. D.. Bruce, P.. Westerhoff, A.. Brawley-Chesworth, Removal of 2-methylisoborneol and geosmin in surface water treatment plants in Arizona, J. Water Supply: Res. and Technol.-Aqua., 51(4), 183-197(2002).
7. H. J.. Lee, H. J.. Son, J. S.. Roh, S. W.. Lee, K. W.. Ji, P. J.. Yoo, L. S.. Kang, Removal of odorous compounds using ozone and hydrogen peroxide, J. Kor. Soc. Environ. Eng., 28(12), 1323-1330(2006).
8. T.. Kim, B.. Moon, T.. Kim, M.. Kim, K.. Zoh, Degradation mechanisms of geosmin and 2-MIB during UV photolysis and UV/chlorine reactions, Chemosphere., 162, 157-164(2016).  9. J.. Park, H.. Nam, J.. Choi, J.. Ha, S.. Lee, Oxidation of geosmin and 2-methylisoborneol by the photo-fenton process: kinetics, degradation intermediates, and the removal of microcystin-LR and trihalomethane from Nak-Dong River water, South Korea, Chem. Eng. J., 313, 345-354(2017).  10. H. J.. Lee, H. J.. Son, C. W.. Lee, S. D.. Bae, L. S.. Kang, Effects of activated carbon types and service life on removal of odorous compounds: geosmin and 2-MIB, J. Korean Soc. Environ. Eng., 29(4), 404-411(2007).
11. J.. Yu, M.. Yang, T.. Lin, Z.. Guo, Y.. Zhang, J.. Gu, S.. Zhang, Effects of surface characteristics of activated carbon on the adsorption of 2-methylisoborneol (MIB) and geosmin from natural water, Sep. Purif. Technol., 56, 363-370(2007).  12. Y.. Matsui, S.. Nakao, A.. Sakamoto, T.. Taniguchi, L.. Pan, T.. Matsushita, N.. Shirasaki, Adsorption capacities of activated carbons for geosmin and 2-methylisoborneol vary with activated carbon particle size: effects of adsorbent and adsorbate characteristics, Water Res., 85, 95-102(2015).  13. E.. Namkung, B. E.. Rittmann, Removal of taste and odour-causing compounds by biofilms grown on humic substances, J. Am. Water Works Assoc., 79(7), 107(1987).
14. R.. Nerenberg, B. E.. Rittmann, W. J.. Soucie, Ozone/biofiltration for removing MIB and geosmin, J. Am. Water Works Assoc., 92(12), 85-95(2000).
15. S. L. N.. Elhadi, P. M.. Huck, R. M.. Slawson, Impact of biomass concentrations on the removal of earthy/musty odors from drinking water by biological filters, Proceedings of 2004 AWWA Annual Conference, June 13~17, Orlando, Florida(2004).
16. K. J.. Meyer, R. S.. Summers, P.. Westerhoff, D.. Metz, Biofiltration for geosmin and MIB removal, Proceedings of 2004 AWWA Annual Conference, June 13~17, Orlando, Florida(2004).
17. B. E.. Rittmann, C. J.. Gantzer, A.. Montiel, Biological treatment to control taste and odor compounds in drinking water. Advances in Taste and Odor Treatment and ControlI. H.. Suffet, J.. Mallevialle, E.. Kawczynsky(Eds.), AWWA Res. Fdn., Denver(1995).
18. H. J.. Son, S. J.. Yoo, J. S.. Roh, P. J.. Yoo, Biological activated carbon (BAC) in water treatment, J. Korean Soc. Environ. Eng., 31(4), 308-323(2009).
19. S. M.. Korotta-Gamage, A.. Sathasivan, A review: potential and challenges of biologically activated carbon to remove natural organic matter in drinking water purification process, Chemosphere., 167, 120-138(2017).  20. D.. Urfer, Effects of Oxidants on Drinking Water Biofilters, PhD thesis Dept. of Civil Engineering, University of Waterloo, ON, Canada(1998).
21. G.. Tchobanolous, F. L.. Burton, Wastewater Engineering: Treatment, Disposal and Reuse, 3rd Edition., McGraw-Hill Inc, , New York(1991).
22. H. J.. Lee, L. S.. Kang, Analysis of geosmin and 2- MIB in water by stir bar sorptive extraction (SBSE) and GC/MS, J. Korean Soc. Environ. Eng., 31(1), 64-69(2009).
23. S.. Velten, F.. Hammes, M.. Boller, T.. Egli, Rapid and direct estimation of active biomass on granular activated carbon through adenosine tri-phosphate (ATP) determination, Water Res., 41, 1973-1983(2007).  24. J. A.. Fuhrman, F.. Azam, Thymidine incorporation as a measure of heterotrophic bacterio-plankton production in marine surface waters: evaluation and field results, Mar. Biol., 66, 109-120(1982).  25. T. R.. Parsons, Y.. Maita, C. M.. Lalli, A Manual of Chemical and Biological Methods for Seawater Analysis Pergamon, New York(1984).
26. R. T.. Bell, G. M.. Ahlgren, I.. Ahlgren, Estimating bacterioplankton production by the [3 H]thymidine incorporation in a eutrophic Swedish Lake, Appl. Environ. Microbiol., 45, 1709-1721(1983).
27. D. M.. Moll, R. S.. Summers, A. C.. Fonseca, W.. Matheis, Impact of temperature on drinking water biofilter performance and microbial community structure, Environ. Sci. Technol., 33(14), 2377-2382(1999).  28. C. C.. Young, I. H.. Suffet, Development of a standard method-analysis of compounds causing taste and odors in drinking water, Water Sci. Technol., 40(6), 279-285(1999).  29. S. W.. Jung, K. H.. Baek, M. J.. Yu, Treatment of taste and odor material by oxidation and adsorption, Water Sci. Technol., 49(9), 289-295(2004).
30. H. J.. Son, H. K.. Park, S. A.. Lee, E. Y.. Jung, C. W.. Jung, The characteristics of microbial community for biological activated carbon in water treatment plant, J. Korean Soc. Environ. Eng., 27(12), 1311-1320(2005).
31. M.. Drikas, M.. Dixon, J.. Morran, Removal of MIB and geosmin using granular activated carbon with and without MIEX pre-treatment, Water Res., 43, 5151-5159(2009). 
|
|















